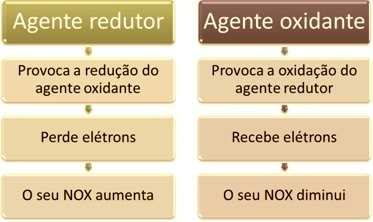
En av huvudfunktionerna som skiljer en oxidationsreduktionsreaktion (eller redox) av de andra är närvaron av ett oxidationsmedel och ett reduktionsmedel, som kan definieras enligt följande:
Titta till exempel på den kemiska reaktionen nedan där aluminium (Al) korroderar i vattenhaltig saltsyralösning (HCl). Aluminiumatomer överför elektroner till H-katjoner+(här) och producera Al-katjonen3+(här):
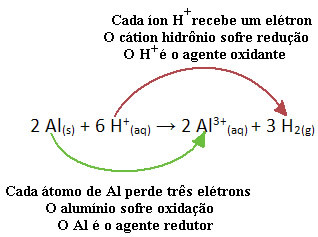
Observera att eftersom Al överförde elektroner betyder det att han orsakade minskningen av H-katjonerna+(här); det är därför han kallas reduktionsmedel. Redan katjonen H+(här) tog bort elektronerna från aluminium, orsakar oxidation av den metallen; därför fungerar han som en oxidationsmedel.
I vardagen finns det många exempel på prestanda hos oxidationsmedel och reduktionsmedel. Titta på några av dem och kom dock ihåg att reduktionen i alla fall sker samtidigt med oxidationen; därför finns det också ett oxidationsmedel om det finns ett reduktionsmedel.
- Exempel på reduktionsmedel:
- I fotografiska filmer: fotografiska filmer innehåller ljuskänsliga silversalter. Vid platser där det förekommer ljus minskar Ag-jonerna+, vilket resulterar i kontrasten observerad i negativ.

- C-vitamin: C-vitamin (L-askorbinsyra) är ett kraftfullt reduktionsmedel i vattenlösning. Den har en exceptionell anläggning som ska oxideras och det är därför den används i stor utsträckning, särskilt i livsmedel som t.ex. antioxidant, det vill säga det tillsätts till andra livsmedel och skyddar dem från eventuell oxidation på grund av dess egna offra. Ett exempel är frukter som äpplen och päron som mörknar i kontakt med syre i luften eftersom de oxiderar. Men när du lägger till en liten mängd apelsin- eller citronsaft (som innehåller vitamin C) till frukten skärs, detta förhindrar att denna reaktion inträffar, eftersom C-vitamin fungerar som ett reduktionsmedel och oxiderar före frukten.

- Vätgas: vätgas (H2) används i raketdrivning och anses vara ett av de viktigaste energialternativen, eftersom dess förbränning frigör en stor mängd energi och inga föroreningar. I denna reaktion fungerar väte som ett reduktionsmedel och oxideras av syre.
- Exempel på oxidationsmedel:
- Vid produktion av vinäger: när vin utsätts för luft förvandlas det till ättika, vars huvudkomponent är ättiksyra. Detta beror på att etylalkoholen eller etanolen i vin oxiderar vid kontakt med atmosfäriskt syre, vilket resulterar i ättiksyra. Således är syre ett oxidationsmedel. Till och med ursprunget till termen "oxidation" är relaterat till reaktionen med syre.

- I rost: såsom anges i föregående exempel verkar syre som ett oxidationsmedel för alkohol; och det gör det också i kontakt med olika metaller, såsom järn, vilket orsakar rostprocessen. Förutom syre i luften är andra oxidationsmedel i detta fall vatten eller en sur lösning.
- I blekmedel: blekningseffekten av blekningarna beror på närvaron av följande två reduktionsmedel: o hypokloritanjon (vanligtvis i form av natriumsalt - NaOCl), närvarande till exempel i blekmedel; och väteperoxid (H2O2), marknadsförs som väteperoxid. Dessa två föreningar har en mycket stark tendens att oxidera och orsaka minskning av andra kemiska arter. Därför är de ansvariga för oxiderande ämnen som ger produkterna mörk färg. I cellulosa bryts till exempel ned lignin och blir lättare och smidigare. Vid fläckborttagning och tygblekning orsakar dessa oxidationsmedel oxidation av organiska molekyler såsom fetter och färgämnen.

- I andningsapparater: en enkel andningsapparat för engångsbruk består av ett klart rör innehållande en vattenlösning av dikromatsaltet av kalium och kiseldioxid, fuktat med svavelsyra; blandad med orange färg. Detta salt, i kontakt med alkoholångan i den berusade förarens andedräkt, reagerar och ändrar färgen till grön. Detta innebär att oxidation av etanol (alkohol) till etanol orsakas.

Av Jennifer Fogaça
Examen i kemi
Källa: Brazil School - https://brasilescola.uol.com.br/quimica/conceito-exemplos-agente-redutor-agente-oxidante.htm

