DE nihonium, atomnummer 113 och symbolen Nh, är ett kemiskt grundämne som tillhör grupp 13 i det periodiska systemet. Dessutom är det ett supertungt element som inte finns i naturen. Således kan dess erhållande endast göras på konstgjord väg, genom kärnfusionsreaktioner. De kemiska egenskaperna hos nihonium är fortfarande inte så tydliga, men det spekuleras i att det beter sig på samma sätt som sin lättare motsvarighet, tallium, i vissa fall.
Nihonium erhölls initialt genom smältning 70Zn med 209Bi, vid Riken Institute, Japan, 2003. Även om ryska och amerikanska forskare också bad om att bli erkända som upptäckare av element 113, erkände IUPAC de japanska forskarna. Namnet syftar på ordet Nihon, som japanerna kallar sitt hemland.
Läs också: Gallium — ett annat kemiskt element som tillhör grupp 13 i det periodiska systemet
sammanfattning om nihonium
Det är ett syntetiskt kemiskt element som finns i grupp 13 av Periodiska systemet.
Dess produktion började 2003, vid Riken Institute, Japan.
Det utgör den grupp av grundämnen som senast ingick i det periodiska systemet, 2015.
Hans studier är fortfarande mycket nya, men vissa försöker koppla det till andra element i grupp 13, som tallium.
Dess produktion är Kärnfusion, med hjälp av isotoper av 70Zn och atomer av 209Bi.
Nihonium egenskaper
Symbol: nä
Atomnummer: 113
Atomisk massa: mellan 278 och 286 c.u. (inofficiell av Iupac)
Elektronisk konfiguration: [Rn] 7s2 5f14 6d10 7 sid1
Mest stabila isotopen:286Nh (9,5 sekunder av halva livet, som kan öka med 6,3 sekunder eller minska med 2,7 sekunder)
Kemisk serie: grupp 13, supertunga element
egenskaper hos nihonium
Nihonium, symbol Nh och atomnummer 113, var ett av de sista grundämnena som ingår i det periodiska systemet. Dess officiellisering skedde den 30 december 2015 av International Union of Pure and Applied Chemistry (IUPAC), medan dess namn gjordes officiellt först i mitten av 2016.
Grundämnen i denna region av det periodiska systemet är mycket instabila, vilket betyder att de inte kan hittas i naturen. Sålunda, inför en påstådd existens, skulle de genomgå radioaktivt sönderfall nästan omedelbart - utsläpp av kärnpartiklar, såsom α och β - för att uppnå större stabilitet.
Men när de släpper ut kärnpartiklar, slutar de med att genomgå kärntransmutation, det vill säga de blir ett nytt kemiskt element. Alltså måste supertunga grundämnen, såsom Nh, produceras i laboratoriet, vilket gör det till en syntetiskt kemiskt element.
Nh, liksom andra supertunga element, påverkas av relativistiska effekter — på ett enkelt sätt avstånd från det som observeras till det förväntade, på grund av relativitet. Således påpekade matematiska studier inom det teoretiska området, som simulerar konsekvenserna av den relativistiska effekten, att nihonium kunde interagera svagt med kvarts, men att ha bra adsorption till guld-, liksom dess lättare motsvarighet, tallium (Tl).
Preliminära teoretiska studier indikerade också flyktighet från Nh. När det gäller adsorption till kvarts bildar tallium lätt TlOH, till exempel, och nihonium misstänks göra detsamma.
Trots det, hur studier är fortfarande mycket preliminära och nya, mycket av det som har producerats är öppet för diskussion, och det är svårt att exakt bestämma nihoniums fysikalisk-kemiska egenskaper.
Att få Nihonium
Element 113, fram till idag, har erhållits på två sätt: genom kalla fusionsreaktioner, med fusion av zink (Zn, Z = 30) med vismut (Bi, Z = 83), och även genom alfasönderfall av element 115.
I det första exemplet är zink accelereras till 10 % av ljusets hastighet, för att övervinna de två kärnornas frånstötande krafter. En isotop produceras då 279Nh, som slutar med att sända ut en neutron och producera 278Nh.

Med en halveringstid på cirka 34 millisekunder är isotopen 278Nh genomgår sex alfasönderfall (alfapartikelutsläpp) till grundämnet mendelevium (Md).
I det andra fallet uppstår element 113 från alfasönderfallet av element 115 (nu känt som muscovium) efter att det har syntetiserats. Ett sätt är den heta fusionsreaktionen av joner 48Ca med isotoper 243ah, producerar 288Mc och sedan, genom alfasönderfall, den 284Nh, som fortsätter att genomgå alfasönderfall.
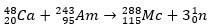
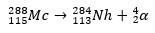
Se också: Hassium — det tyngsta syntetiska kemiska grundämnet för att få sina egenskaper analyserade
nihoniums historia
Sökningarna efter element 113 började 2003. Japanska forskare vid Rikeninstitutet accelererade isotoper av 70Zn vid 10% av ljusets hastighet för att kollidera med 209Bi, genom en fusionsreaktion. Därmed lyckades de producera det vi nu känner som 278Nh.
Det var dock först 2012 som Japanska forskare kunde upptäcka hela alfasönderfallsserien av element 113, kontakta IUPAC för att göra anspråk på upptäckten.
Samtidigt med japanska ansträngningar, ryska forskare ledda av Yuri Oganessian, i samarbete med Amerikanska forskare, kom också att identifiera elementet 113 genom alfasönderfall av elementet 115. Sådana experiment ställer också ryska och amerikanska vetenskapsmän i strid om erkännande av element 113.

IUPAC fann dock att bevisen från Riken-institutet var mer solida, och så tillät japanerna att ha rätt att namnge element 113. Namnet som valdes var nihônio, symbol Nh, med hänvisning till landet Japan. Ordet Japan är skrivet av japanerna med två kinesiska tecken som betyder "den stigande solens land" och läses som Nihon eller Nippon.
Namnet nihonium valdes också eftersom den japanska kemisten Masataka Ogawa 1908 publicerade att hade upptäckt element 43 och döpte det japanskt, symbol Np (som idag tillhör neptunium, Z = 93). Senare bevisades det dock att element 43 var instabilt, inte fanns i naturen och syntetiserades först 1937 och fick namnet på teknetium (Tc).
Således försvann japanska från det periodiska systemet. Men år senare bevisades det att Ogawa faktiskt hade upptäckt element 75 (nu känt som renium). Men vid den tiden hade grundämnet rhenium redan officiellt upptäckts 1925 och döpts.
Lösta övningar på nihonium
fråga 1
Nihonium, symbol Nh och atomnummer 113, är ett kemiskt grundämne som inte kan hittas i naturen på grund av dess korta halveringstid. Den mest uthålliga av dem, den 286Nh, har cirka 9,5 sekunder. Att veta att halveringstid är den tid som krävs för att mängden av arten ska halveras, hur många sekunder tar det för mängden av ovanstående isotop att vara 1/16 av mängden första?
A) 9,5
B) 19
C) 28,5
D) 38
E) 47,5
Upplösning:
Alternativ D
Var 9,5:e sekund sjunker mängden av isotopen med hälften. Så efter 9,5 sekunder är dess mängd hälften av det ursprungliga beloppet. Ytterligare 9,5 sekunder, totalt 19 sekunder, sjunker mängden med hälften igen och når 1/4 av initialen.
Vid 28,5 sekunder, efter ytterligare en halveringstid, sjunker mängden med hälften igen och når 1/8 av den initiala mängden. Slutligen, efter 38 sekunder, sjunker beloppet med hälften igen och når 1/16 av det ursprungliga beloppet, som begärts i uttalandet. Tiden som krävs är alltså 38 sekunder.
fråga 2
År 2003 började sökandet efter element 113 vid Riken Institute i Japan. Vid den tiden kunde forskare producera 278Nh genom fusion av zink- och vismutatomer.
Hur många neutroner finns i den citerade isotopen?
A) 113
B) 278
C) 391
D) 170
E) 165
Upplösning:
Alternativ E
Antalet neutroner kan beräknas som:
A = Z + n
där A är antalet pasta atom-, Z är atomnumret och n är antalet neutroner. Genom att ersätta värdena har vi:
278 = 113 + n
n = 278 - 113
n = 165
Av Stefano Araújo Novais
Kemilärare

