Oxidation är namnet på processen för förlust av elektroner av en atom, grupp eller jonart under a kemisk reaktion. Det identifieras från ökningen av NOX (oxidationstal) för arten eller atomen när man jämför reaktant och produkt.
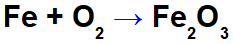
Järnoxidationsekvationen.
I ekvationen ovan kan vi till exempel ange NOX för var och en av deltagarna:
Reagensjärn (Fe): har NOX 0 eftersom det är en enkel substans;
Syre i reagens (O): har NOX 0 eftersom det är ett enkelt ämne;
Syre i produkten: den har NOX -2 eftersom den inte är kopplad till en alkalimetall, jordalkali eller vätebildande peroxider eller superoxider;
Järn i produkten: den har NOX +3 eftersom summan av NOX för järn multiplicerat med 2 (antal atomer) + NOX av syre multiplicerat med 3 måste resultera i 0 eftersom det är ett sammansatt ämne:
x, 2 + 3.(-2) = 0
2x - 6 = 0
2x = +6
x = + 6
2
x = +3
När vi jämförde NOX för reagensjärnet (0) med produkten (+3), observerade vi en ökning, det vill säga den genomgick processen med oxidation. Det är värt att notera att förekomsten av
oxidation det åtföljs alltid av fenomenet reduktion (vilket betyder förstärkning av elektroner), identifierat av minskningen av NOx, som sker med syre i exemplet.Läs också:Bestämning av oxidationstal (NOX)
Exempel på situationer där oxidation inträffar:
1. Förbränning

Förbränningen av ett material tyder också på oxidation.
Förbränning är varje kemisk reaktion som sker i närvaro av en bränsle någon och den oxiderande syrgasen (O2), vilket resulterar i produktion av värme och ljus. I varje förbränningsreaktion inträffar oxidation.
2. Vissa organiska reaktioner
I varje organisk reaktion som äger rum i närvaro av de medel som anges nedan, processen av oxidation:
Kaliumdikromat (K2Cr2O7) eller kaliumpermanganat (KMnO4);
Närvaro av stark syra eller stark bas;
Ozongas (O3) i närvaro av metalliskt zink (Zn) och vatten (H2O).
3. Batterier eller batterier

Batterier är enheter där oxidation alltid sker.
Stackar eller batterier är elektrokemiska enheter som lagrar kemiska ämnen. En av dessa ämnen kommer att genomgå oxidation, och den andra kommer att genomgå reduktion, vilket resulterar i produktion av elektrisk ström.
4. Elektrolys
Elektrolys är en kemisk process där en vattenlösning innehållande ett salt utsätts för en elektrisk ström, vilket slutar med att främja oxidationen av anjoner som finns i dessa material. I all elektrolys finns det oxidation.
Av mig Diogo Lopes Dias
Källa: Brasilien skola - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-oxidacao.htm

