Kolloider, kolloidala lösningar eller kolloidalt system är blandningar som visar utseendet på en lösning, det vill säga en homogen blandning. Men faktiskt är de heterogena blandningar.
Detta beror på att även om det inte är klart för blotta ögat, kan skillnaden i kolloidala blandningar observeras genom användning av instrument som mikroskopet.
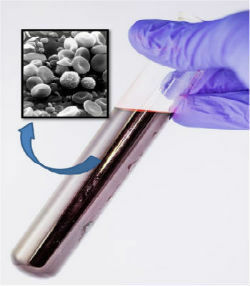 Blodet, trots att det verkade homogent, med användning av ett mikroskop observerade vi att det består av flera komponenter.
Blodet, trots att det verkade homogent, med användning av ett mikroskop observerade vi att det består av flera komponenter.
Kolloider finns i våra dagliga liv. Dom är exempel på kolloider: fuktkräm, yoghurt, mjölk, blod, färgämnen och sylt.
Det är av denna anledning som vissa kemiska produkter indikerar att de måste skakas innan de används. Detta måste göras för att förena kolloidala partiklar.
Samtidigt sedimenterar inte kolloidala blandningar naturligt. Om vi lägger en kolloid i en behållare sätter sig inte partiklarna i botten. De kan inte heller filtreras.
Storleken på partiklar som finns i kolloider är mellan 1 och 100 nanometer (1 nanometer motsvarar 1 miljonedel av en millimeter).
Allt utanför detta intervall är homogena eller heterogena blandningar.
Homogena blandningar anses vara verkliga lösningar. Dess partiklar är mindre än 1 nanometer. Heterogena blandningar har partiklar större än 100 nanometer.
Lära sig mer om Kemiska lösningar och Separation av blandningar.
Vilka är dina fastigheter?
Komponenterna i kolloider kallas spridd och dispergeringsmedel. Mängden dispergeringsmedel är alltid högre.
Tydligen antar de en homogen blandningskaraktäristik.
Ett exempel är äggvitor som slås i snö: vit i flytande form tar rollen som dispergerad komponent.
Luften, som fick den vita att förvandlas till ett skum, är den spridande komponenten, eftersom det tog mer luft än den vita för att uppnå denna blandning.
Dessutom tillåter kolloider att ljus passerar mellan dem, vilket inte är fallet med homogena blandningar.
Om vi riktar en ficklampa med en liten ljusstråle mot en kolloidal blandning är det möjligt att se en ljusstråle passera genom hela behållaren där den är placerad. Det är vad det heter Tyndall-effekt.
Genom samma experiment är det också möjligt att detektera den slumpmässiga rörelsen av partiklar i blandningen. Det här kallas Brownsk rörelse.
Kort sagt, egenskaper hos kolloidala system dom är:
- Blandningens faser är inte lätt att skilja.
- Partikelstorleksintervallet är 1 och 100 nanometer;
- Tyndall-effekt;
- Närvaro av dispergerade partiklar och dispergeringsmedel;
- De löser sig inte naturligt och kan inte filtreras;
- Brownsk rörelse.
Typer av kolloider
Kolloider klassificeras enligt det fysiska tillståndet hos spridda och spridande partiklar.
Typerna av kolloider är: aerosol, emulsion, skum, gel och sol (de som ser ut som en lösning). Läs mer om var och en av dem:
Aerosol
Dispergerad komponent: Fast eller flytande
Dispergeringskomponent: gas
Exempel: Rök, dimma, moln, spray
Emulsion
Dispergerad komponent: Vätska
Dispergeringskomponent: Flytande eller fast
Exempel: Majonnäs, smör, ost, glass
Skum
Dispergerad komponent: gas
Dispergeringskomponent: Flytande eller fast
Exempel: Vispad grädde, vit i snö, rakskum, popcorn
Gel
Dispergerad komponent: Vätska
Dispergeringskomponent: fast
Exempel: Gelatin, kiselgel, tandkräm
Sol
Dispergerad komponent: fast
Dispergeringskomponent: Flytande eller fast
Exempel: Pearl, Ruby, Blood
För att lära dig mer, lär dig mer om en metod för att separera kolloidala blandningar Centrifugering.