Kemisk isomerism är ett fenomen som observeras när två eller flera organiska ämnen har samma molekylformel, men olika molekylstruktur och egenskaper.
Kemiska ämnen med dessa egenskaper kallas isomerer.
Termen kommer från de grekiska orden iso = lika och bara = delar, det vill säga lika delar.
Det finns olika typer av isomerism:
- platt isomer: Föreningar identifieras med platta strukturformler. Det är uppdelat i kedjeisomerism, funktionsisomerism, positionisomerism, kompensationsisomerism och tautomerismisomerism.
- rymdisomer: Föreningarnas molekylära struktur har olika rumsliga strukturer. Den är uppdelad i geometrisk och optisk isomerism.
platt isomer
På platt isomerism eller konstitutionell isomerism, är den organiska substansernas molekylära struktur platt.
Föreningar som uppvisar denna egenskap kallas platta isomerer.
kedjeisomer
Kedjeisomerism händer när kolatomer har olika kedjor och samma kemiska funktion.
Exempel:
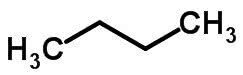
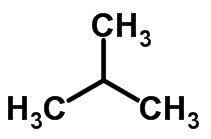
Funktion Isomerism
Funktionsisomerism uppstår när två eller flera föreningar har olika kemiska funktioner och samma molekylformel.
Exempel: Detta fall är vanligt mellan aldehyder och ketoner.
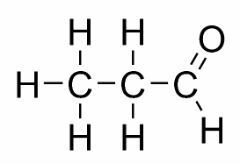
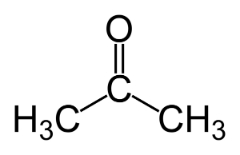
Positionsisomer
Positionsisomerism uppstår när föreningar differentieras genom olika omättnad, förgrening eller funktionella grupppositioner i kolkedjan. I detta fall har isomererna samma kemiska funktion.
Exempel:

kompensering av isomer
Kompensationsisomerism eller metamerism förekommer i föreningar med samma kemiska funktion som skiljer sig åt av heteroatomen.
Exempel:

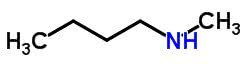
Tautomery
Tautomerism eller dynamisk isomerism kan betraktas som ett specifikt fall av funktionsisomerism. I detta fall kan en isomer förändras till en annan genom att ändra positionen för ett element i kedjan.
Exempel:

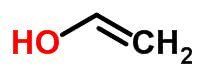
rymdisomer
DE rymdisomerism, även kallad stereoisomerism, händer när två föreningar har samma molekylformel och olika strukturformler.
I denna typ av isomerism fördelas atomer på samma sätt men upptar olika positioner i rymden.
geometrisk isomer
DE geometrisk isomerism eller cis-trans förekommer i omättade öppna kedjor och även i cykliska föreningar. För att göra detta måste kolliganderna vara olika.

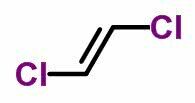
- När samma ligander är på samma sida får isomernomenklaturen prefixet cis.
- När samma ligander är på motsatta sidor får nomenklaturen prefixet trans.
IUPAC (International Union of Pure and Applied Chemistry) rekommenderar att bokstäverna Z och E används som prefix istället för cis och trans.
Detta beror på att Z är den första bokstaven i det tyska ordet zusammen, vilket betyder "tillsammans". Och det är den första bokstaven i det tyska ordet entegegen, vilket betyder "motsatt".
optisk isomer
DE optisk isomerism demonstreras av föreningar som är optiskt aktiva. Det händer när ett ämne orsakas av vinkelavvikelsen i planet för polariserat ljus.
- När ett ämne böjer optiskt ljus till höger kallas det högerhänt.
- När ett ämne böjer optiskt ljus åt vänster kallas ämnet levorotary.
Ett ämne kan också finnas i två former som är optiskt aktiva, dextogyra och levogyra. I det här fallet kallas det enantiomer.
För att en kolförening ska vara optiskt aktiv måste den vara kiral. Detta innebär att deras ligander inte kan överlappa varandra, eftersom de är asymmetriska.
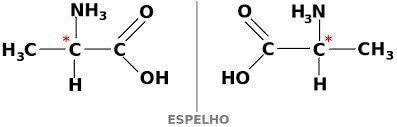
I sin tur, om en förening har dextrogyra- och levorotära former i lika delar kallas de racemiska blandningar. Den optiska aktiviteten hos racemiska blandningar är inaktiv.
Läs också:
- Kol
- Organisk kemi
- Molekylär formel
- Strukturformel
Övningar
1. (Mackenzie 2012) Nummerkolumn B, som innehåller organiska föreningar, som associerar dem med kolumn A, enligt den typ av isomerism som varje organisk molekyl presenterar.
Kolumn A
1. kompensering av isomer
2. geometrisk isomer
3. kedjeisomer
4. optisk isomer
Kolumn B
() cyklopropan
() etoxietan
() bromklor-fluor-metan
() 1,2-dikloreten
Den korrekta siffran i kolumn B, från topp till botten, är
a) 2 - 1 - 4 - 3.
b) 3 - 1 - 4 - 2.
c) 1 - 2 - 3 - 4.
d) 3 - 4 - 1 - 2.
e) 4 - 1 - 3 - 2.
Alternativ b) 3 - 1 - 4 - 2.
2. (Uerj) Isomery är fenomenet som kännetecknas av det faktum att samma molekylformel representerar olika strukturer.
Med tanke på den platta strukturella isomerismen för molekylformeln C4H8kan vi identifiera isomerer av följande typer:
a) kedja och position
b) kedja och funktion
c) funktion och kompensation
d) position och ersättning
Alternativ a) sträng och position
3. (OSEC) Propanon och isopropenol exemplifierar ett fall av isomerism:
a) av metameria
b) funktion
c) av tautomery
d) cis-tran
e) kedja
Alternativ c) för tautomery
Se också: Övningar på platt isomerism
