Det kan hända att det finns syror av samma element, och detta element har samma oxidationsnummer (NOX), men skillnaden är i hydratiseringsgraderna.
Till exempel nedan har vi tre syror bildade av grundämnet fosfor (P):
H3DAMM4 H4P2O7 HPO3
Observera att i alla tre syrorna är oxidationsantalet av fosfor +5; skillnaden ligger i hydratiseringsgraden.
Baserat på detta differentieras dessa syror i nomenklaturen genom prefixen orto, pyro och meta.
Den mest hydratiserade syran kallas orto. I det givna exemplet är den första (H3DAMM4) kallas syra ortofosforsyra, eftersom det är den mest hydratiserade av de tre. Orto-prefixet är förbrukat, så för det mesta kommer denna syra bara att kallas fosforsyra.
Prefixen pyro och meta används med ortosyra som referenspunkt:
- Pyrus: 2 molekyler orto minus 1 molekyl H.2O
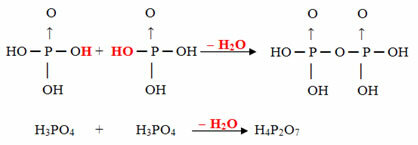
Exempel: H4P2O7 kallas syra pirofosforsyra eftersom det är lika med två molekyler ortofosforsyra (H3DAMM4) minus en vattenmolekyl.
2. H3DAMM4 = H6P2O8
H6P2O8 - H2O = H4P2O7
Denna process är en intermolekylär uttorkning:
- Mål: 1 molekyl orto minus 1 molekyl H.2O
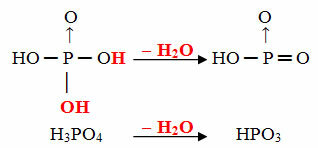
Exempel: HPO3 kallas syra målfosforsyra eftersom den är lika med en molekyl ortofosforsyra (H3DAMM4) minus en vattenmolekyl.
H3DAMM4 - H2O = HPO3
Denna process är en intramolekylär uttorkning:
Av Jennifer Fogaça
Examen i kemi
Källa: Brazil School - https://brasilescola.uol.com.br/quimica/grau-hidratacao-dos-acidos.htm

