Atomvolymen är inte den volym som en atom upptar, utan avser den volym upptagen av en fast kvantitet av ett givet antal atomer av ett kemiskt element.
I texten Kemiskt element, visades att ett element motsvarar en uppsättning atomer som har samma atomnummer, det vill säga samma mängd protoner i kärnan. Mängden som fastställts för att beräkna atomvolymen är värdet av Avogadro är konstant, vilket är lika med 6,02. 1023 atomer, vilket motsvarar 1 mol av elementet.
Så vi kan säga det atomvolymen är den volym som 1 mol atomer (eller 6,02). 1023 atomer) av ett element upptar.
Denna kvantitet kan beräknas om vi känner till densiteten hos solid state-elementet och massan av 1 mol atomer i det elementet. Tänk till exempel att densiteten av natrium (Na) är lika med 0,97 g / cm3 och den 6.02. 1023 natriumatomer har en massa lika med 23,0 g. Vi kan sedan, från formeln för densitet, komma fram till atomvolymen av natrium. Se hur:
densitet = pasta
volym
atomvolym = massa 6,02. 1023 elementatomer
solid state element densitet
Atomvolym av natrium = 23,0 g
0,97 g / cm3
Atomvolymen av natrium = 23,71 cm3
Atomvolymvärdet involverar inte bara atomernas storlek utan också avståndet mellan dem. Eftersom det också innefattar tomma utrymmen, vi kan inte ta atomvolymvärdet och dela med antalet atomer (6.02. 1023) för att hitta volymen som varje atom upptar.
Sluta inte nu... Det finns mer efter reklam;)
Det är viktigt att studera atomvolymen eftersom den är en periodisk egenskap, det vill säga den varierar beroende på grundämnets atomnummer. Titta på bilden nedan. Elementens atomvolym växer från topp till botten, vilket innebär att när vi analyserar elementen som tillhör samma familj i det periodiska systemet, när atomantalet växer, växer också atomvolymen. Detta beror på att perioderna i denna mening ökar, vilket innebär att atomernas elektroniska lager ökar och följaktligen också volymen som upptar dem ökar. Detta är samma känsla av tillväxt som atomstråle.
Å andra sidan ser vi horisontellt att atomvolymen ökar från mitten till kanterna. När vi börjar från vänster och går höger till mitten av det periodiska systemet minskar atomvolymen eftersom perioden är samma, det vill säga elementen i samma linje har samma mängd elektroniska lager, men atomnumret kommer ökande. Detta innebär att mängden elektroner ökar i denna riktning, vilket resulterar i en större kraft på elektroners attraktion till atomkärnan, vilket minskar dess atomradie och följaktligen volymen atom. Men från centrum till höger fortsätter detta inte att hända, för när det gäller element i denna region, särskilt när det gäller icke-metaller är avståndet mellan deras atomer relativt stort, vilket påverkar atomvolymen, öka den.
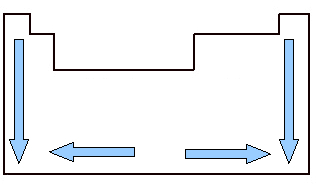
Atomvolymvariation i det periodiska systemet över familjer och perioder
Av Jennifer Fogaça
Examen i kemi


