Polymerisation är namnet på den kemiska processen som resulterar i bildandet av makromolekyler (stora molekyler) som kallas polymerer, genom kombinationen av mindre molekyler, monomererna.
reaktionen av polymerisation det är mycket vanligt i naturen, som vi kan se i kolhydrater (som stärkelse) och proteiner (som kasein i mjölk). Det förekommer också syntetiskt, eftersom den stora majoriteten av polymerer som används av människor i deras dagliga liv tillverkas konstgjort.
Den första polymeren framställd av polymerisation syntetisk var bakelit 1909 av den belgiska kemisten Leo Hendrik Baekeland.
I allmänhet för att en monomer ska kombineras med en annan (oavsett om de är desamma eller olika) i en reaktion av polymerisation, är det nödvändigt förekomsten av fri valens (kemisk bindning som ska utföras) i båda monomererna.
Dessa valenser uppstår som ett resultat av att bindningar bryts genom användning av katalysatorer (såsom nickel), yttre förhållanden såsom ljus och värme, eller genom fenomenet resonans i strukturen (elektronskift).
Vid bildandet av polypropen (PP-polymer), till exempel används i hushållsredskap och leksaker, pi länk (π) i varje molekyl bryts ned enligt följande:
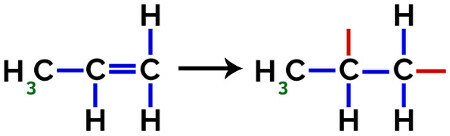
Brott av pi-bindning i propylen
Således kan varje propylenmonomer bindas till två andra propylenmonomerer och bilda polymeren PP eller polypropen (prefixet poly indikerar flera monomerenheter). Det vanligaste sättet att representera en polymer har monomeren mellan parenteser och på utsidan bokstaven n, som indikerar flera monomerer, som vi kan se i fallet med PP-polymeren:
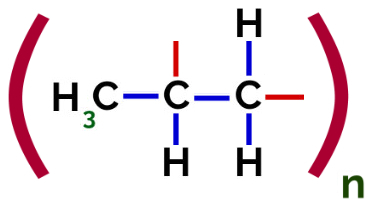
Representation av PP-polymer
reaktionen av polymerisation kan göras på olika sätt, som vi kommer att se nedan:
a) Reaktion av additionspolymerisation
I denna polymerisation, det finns alltid ett brott av en pi-bindning i monomeren, vilket gör att två fria valenser uppträder i strukturen, som vid bildandet av polyeten, polymer som används i stor utsträckning i läkemedelsförpackningar.
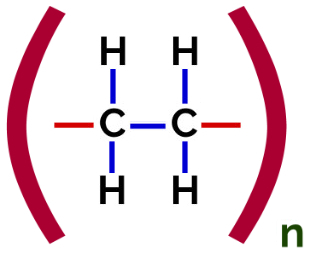
Polyetentillsatspolymerstrukturformel
På polymerisation av polyeten används molekyler av eten (eten) som monomeren, som har en pi-bindning mellan de två kolatomerna. När denna bindning bryts uppträder två fria valenser, en på varje kolatom som var involverad i pi-bindningen. Monomererna förenas exakt i var och en av dessa valenser, det vill säga valens för en är kopplad till valens av den andra, och så vidare.
Sluta inte nu... Det finns mer efter reklam;)
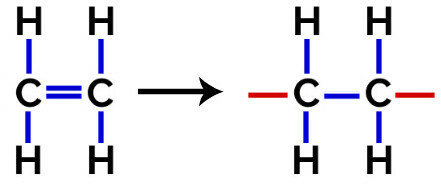
Polyetenbildningsekvation
b) Additionspolymerisationsreaktion 1.4
Vid denna polymerisation presenterar monomererna två alternerande dubbelbindningar (en pi och en sigma), vilket gynnar fenomenet av resonans (alternerande positionen för pi-elektronerna i pi-bindningen), som vid bildandet av syntetiskt gummi (polybutadien)

Strukturformel för polybutadien
Den monomera enheten för denna polymer är butadien, som har två alternerande dubbelbindningar. Med resonans har strukturen en dubbelbindning mellan kol 2 och 3 och två fria valenser på kol 1 och 4. Det är just i dessa fria valenser av kol 1 och 4 som monomererna kombinerar.

Resonans i butadien
c) Reaktion av kondensationspolymerisation eller eliminering
Det är en reaktion av polymerisation i vilka två monomerer (samma eller olika) obligatoriskt samtidigt förlorar atomer eller grupper, vilket resulterar i två fria valenser i var och en av dem. På detta sätt finns det alltid eliminering av väte från en monomer, som sedan förenar en halogen (F, Cl, Br, I), OH, NH2eller till CN för den andra monomeren.
Så, i polymerisation genom eliminering finns det alltid bildning av vatten, halogenerad syra (HCl, HI, HF, HBr), ammoniak (NH3(Hydrocyanic acid (HCN)) förutom polymeren. Se till exempel representationen av bildandet av polyester, ett material som används som tyg:

Polyesterformationsekvation
Polyesterbildande monomerer är p-bensensyra och etan-1,2-diol. Det kan vi se i detta polymerisation eliminering av vattenmolekyler sker, eftersom de två monomererna har två hydroxyler. I denna process förlorar syran de två hydroxylerna och dialkoholen förlorar endast väte från hydroxylerna:

Polyesterstruktur
Polyestermonomerer förenas av syret i alkoholen och kolet i karboxylsyran.
Av mig Diogo Lopes Dias


