Metaller är element som kännetecknas av ljusstyrka, styrka, termisk och elektrisk ledningsförmåga. Dom är tillämpbar i praktiskt taget alla industriella processer, finns i metalllegeringar som används vid tillverkning av verktyg, smycken och mynt och i kemiska processer såsom redox, som ansvarar för driften av staplar och batterier.
I det periodiska systemet klassificeras de i:
halvmetaller
övergångsmetaller
alkaliska metaller
alkaliska jordartsmetaller
Inom stålindustrin är de uppdelade i:
järnmetaller
icke-järnmetaller
tungmetaller
Läs också: Vilka är de nya elementen i det periodiska systemet?
Metallegenskaper

De är för det mesta utmärkta ledare för värme och elektricitet.
De har ett glansigt utseende.
har höga densitet.
De är elektropositiva element (de tenderar att bilda katjoner - positiva laddningar).
Med undantag för Kvicksilver, de är element med hög smältpunkt och fasta vid rumstemperatur.
De har mekanisk hållfasthet (seghet).
De är formbara (kan formas utan att gå sönder).
Sluta inte nu... Det finns mer efter reklam;)
Metaller för periodiska system
alkaliska metaller
Är elementen i första kolumnen i det periodiska systemet, familj 1A. De kallas alkalimetaller eftersom de, när de blandas med vatten, bildar hydroxider, det vill säga en alkalisk (basisk) lösning.
Du element som tillhör denna grupp är:
Litium (li)
Natrium (På)
Kalium (K)
Rubidium (Rb)
Cesium (Cs)
Francium (Fr)
Den elektroniska konfigurationen av alkalimetaller i neutralt (oladdat / joniserat) tillstånd presenteras bara en elektron i det sista skalet (valenslager). O atomstråle och metallernas reaktivitet ökar från topp till botten (observera Periodiska systemet). De har en låg smältpunkt jämfört med andra metaller, är smidiga och inte särskilt täta, har en matt aspekt på grund av hög oxidationspotential.
Se också:Vilka är materiens egenskaper?
alkaliska jordartsmetaller
Dessa är element som visas i andra kolumnen i det periodiska systemet, familj 2A. kallas alkalisk jord av tendensen att bilda lösningar av en grundläggande (alkalisk) karaktär och av jord eftersom oxiderna bildade av dessa ämnen före 1800-talet betecknades så. Denna term användes för att beteckna icke olösliga metaller som inte genomgick mutation vid uppvärmning, vanliga egenskaper hos grupp 2-element. Senare, mot bakgrund av ny forskning och experiment, upptäcktes att "jord" -elementen faktiskt var oxider bildade av metaller.
De är formbara metaller, med låg densitet, har två elektroner i dess yttersta skal, finns under normala temperatur- och tryckförhållanden i fast tillstånd. Tillhör denna grupp:
Beryllium (Vara)
Magnesium (Mg)
Kalcium (Här)
Strontium (Mr)
Barium (Ba)
Radio (Groda)
övergångsmetaller
göra upp grupp B i det periodiska systemetoch är belägna mellan jordalkalimetallerna och ametaler. De definierades av IUPAC som element som har en ofullständig energéticad 'energiska underlag. Termen "övergångsmetaller" refererar till övergång från grupp 2 till 13 i det periodiska systemet och det ökande tillägget av elektroner i d-omloppet.
Övergångsmetallgruppen består av täta element, med höga smält- och kokpunkter, och mindre reaktiva än grupp 1 och 2 metaller (Familj 1A och 2A). Bland övergångsmetallerna är volfram, som är det grundämne som har den högsta smältpunkten (3422 ° C), och kvicksilver (Hg), som är en metall som är flytande under normala temperatur- och tryckförhållanden, dess smältpunkt är (-38,83 ° C).
Övergångsmetaller har olika oxidationstillstånd (NOX variabla) och bildar färgade ämnen.

Interna övergångselement
Interna övergångselement dom är:
Lanthanides: serier som består av element som har 57 till 71 protoner och som, med undantag av prometium, är naturliga.
Actinides: grupp bildad av element som sträcker sig från 89 till 103 i atomnummer och som för det mesta är syntetiska. Alla denna grupp är radioaktiv med kort halveringstid.
Elementen i dessa två grupper har en hög smältpunkt och är alla fasta vid rumstemperatur.
Halvmetaller
Du halvmetaller det finns totalt sju element:
Bor (B)
Kisel (Si)
Germanium (Ge)
Arsenik (As)
Antimon (Må)
Tellurium (Te)
Polonium (Po)
Denna klassificering ges till element som har fysikalisk-kemiska egenskaper som är relevanta för metaller och även andra som är relevanta för icke-metalliska element. Halvmetaller har en glans, är spröda föreningar, som kan bilda katjoner och även anjoner (beroende på tillståndet) och är mellanledare.
Typer av metaller
Järn: ämnen som innehåller järn i sin sammansättning. Dom är metalllegeringar som innehåller järn som ett vanligt element, men kan formuleras med olika koncentrationer av kol, till exempel eller smidda med olika tekniker, och därmed ha produkter med olika fysiska egenskaper.
Icke-järnhaltig: legeringar bildade av andra typer av metaller, såsom aluminium, koppar, nickel, zink, titan.
Tungmetaller: bly, nickel, zink, kvicksilver. De är reaktiva, giftiga och bioackumulerande metaller. De används bland annat i batterier, lampor, ammunition för militära artefakter.
Kemiska bindningar av metaller
Metaller är element elektropositiv, det vill säga de har en tendens att förlora elektroner i en kemisk bindning. När en metall interagerar med en icke-metall, den utföra en jonbindning på grund av skillnaden i elektronnegativitet. Den andra bindningsmöjligheten för metaller är metallbindningar.
På metallanslutningar mellan metaller, med delvis frisättning av elektroner och bildandet av ett moln eller hav av elektroner runt atomerna, vilket garanterar metalldelarna egenskaperna hos ledningsförmåga elektrisk och smidbarhet.
Se också: Ledare och isolatorer - vad är skillnaderna?
Erhålla metaller
De flesta metaller finns naturligt i bergarter och mineraler associerade med andra element. Det finns flera tekniker för raffinering av metaller, såsom genom elektrolys och kemiska reaktioner för att separera föreningar.
När det gäller metaller är de två mest använda teknikerna i industriell skala för att uppnå en viss grad av renhet i en metall: skillnad på densitet och magnetisk känslighet (tendens att metallen måste reagera på en magnetiskt fält).

lösta övningar
Fråga 1 - (Enem) Kadmium, som finns i batterier, kan nå marken när dessa material oregelbundet kasseras i miljön eller när de förbränns. Till skillnad från metallformen är Cd2 + -joner extremt farliga för kroppen eftersom de kan ersätta Ca2 + -joner som orsakar en degenerativ sjukdom i benen, vilket gör dem mycket porösa och orsakar svår smärta i benen. lederna. De kan också hämma enzymer aktiverade av Zn2 + -katjonen, vilket är extremt viktigt för njurarnas funktion. Figuren visar variationen i radien för vissa metaller och deras respektive katjoner.
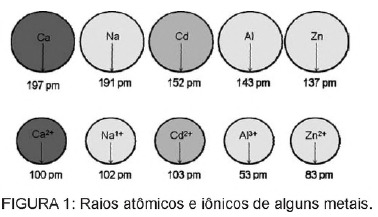
Baserat på texten är giftigheten av kadmium i sin jonform en konsekvens av detta element
A) har låg joniseringsenergi, vilket gynnar bildandet av jonen och underlättar dess bindning till andra föreningar.
B) har en tendens att agera i biologiska processer medierade av metalliska katjoner med laddningar från +1 till +3.
C) har en radie och laddning relativt nära metalljoner som verkar på biologiska processer, vilket orsakar störningar i dessa processer.
D) har en stor jonradie, så att den kan störa biologiska processer där mindre joner normalt deltar.
E) har en +2 laddning, vilket gör det möjligt att störa biologiska processer där normalt joner med lägre laddningar deltar.
Upplösning
Alternativ C. Kadmium är ett element som liknar de metalliska joner som vi naturligt har i kroppen. Förutom att vara bioackumulerande kan kadmium, som har denna likhet med metallgrupper, binda till sulfhydrylgrupper av molekyler protein, vilket orsakar förändringar i biologiska processer, såsom avkalkning, och vävnads- och röda blodkroppar förstörs blod.
Fråga 2 - Kryssa för fel alternativ för egenskaper som är relevanta för metaller.
A) De flesta metaller är bra elektriska och termiska ledare.
B) Vissa metaller är mottagliga för oxidation och / eller reduktion.
C) Järn är en resistent och formbar metall, det vill säga det är lätt att forma.
D) Alkaliska jordartsmetaller har detta namn "jord" med hänvisning till oxiderna av dessa metaller, som är mörka i färg.
E) Metaller är element i olika färger och tråkiga på grund av oxidationsverkan.
Upplösning
Alternativ E. Metaller är naturligt glänsande och metalliska i färg, de kan genomgå oxidation, vilket orsakar förändringar i egenskaperna som är relevanta för aspekt av delen, men detta är inte ett fenomen som händer i alla metaller, och i vissa fall beror oxidation på flera faktorer extern.
av Laysa Bernardes
Kemilärare