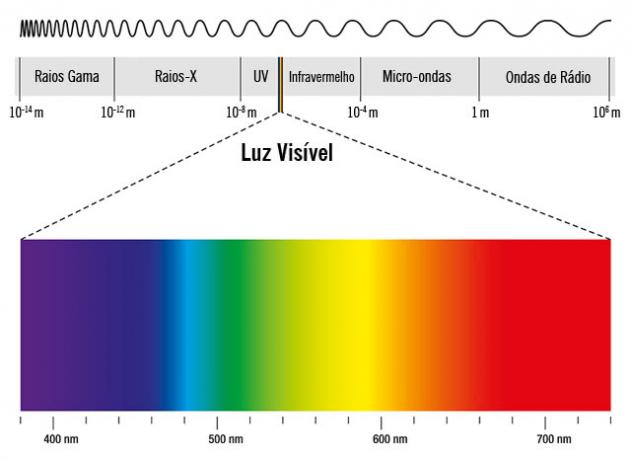
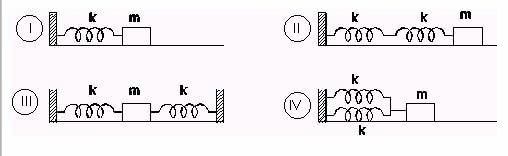
Sedan antiken har människan varit intresserad av att svara på frågan om materiens sammansättning.
Flera personligheter från det vetenskapliga samfundet tog ställning till ämnet, men det var först i slutet av 1800-talet som mysterierna om atomsammansättning började rivas upp.
Den antika filosofen Leucippus, till exempel, trodde att atomen bestod av små partiklar.
Efter denna definition föreslogs det av Democritus och Dalton att atompartiklar var massiva och odelbara.
Detta faktum ifrågasattes senare av Thomson, en engelsk fysiker som upptäckte elektronens existens och sedan kunde bekräfta den idé som Leucipo tidigare föreslog.
Efter denna upptäckt presenterade Thomson en modell där atomen bildades av en sfär med positiva laddningar och inuti kärnan fanns elektroner.
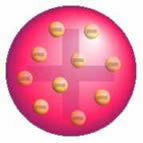
Thomsons Atom Model - I en positivt laddad, jämnt fördelad massfär,
de skulle vara belagda med negativt laddade elektroner, som i pudding.
Till och med efter Thomsons teori hade atommodellen fortfarande en teoretisk-experimentell brist som kunde bevisa dess riktighet.
Ämnet diskuterades återigen varmt när fysiker Rutherfords team noterade att det fanns en mycket stor avvikelse (och oförklarlig, enligt russinpuddingsteorin) när några radioaktiva alfapartiklar passerade genom ett tunt lager av laminat metallisk.
Efter att ha analyserat och studerat faktum kom Rutherford till slutsatsen att atomens radie är 10 000 gånger större än kärnans radie.
Genom hela studien av atomen kom Rutherford och hans team 1911 till en atommodell, som de kallade atommodellen.
Sluta inte nu... Det finns mer efter reklam;)

1913 dechiffrerade Niels Bohr atommodellen och tillämpar den kvantitet av handling som Planck upptäckte i sina studier. Handlingskvantumet var i själva verket det stora jokertecknet som skulle komma att komplettera och förtydliga atommodellen.
Bohr justerade effektivt och enkelt modellen som presenterades av Rutherford och kom till följande slutsats:
Elektronen förvärvar energi, som representeras genom en definierad bana. De tillåtna banorna bildar energinivåerna.

Av Talita A. änglar
Examen i fysik
Brasilien skollag
Fysik Modern - Fysik - Brasilien skola
Vill du hänvisa till texten i en skola eller ett akademiskt arbete? Se:
ÄNGLAR, Talita Alves dos. "Från Rutherfords atom till Bohrs atom"; Brasilien skola. Tillgänglig i: https://brasilescola.uol.com.br/fisica/do-atomo-rutherford-ao-atomo-bohr.htm. Åtkomst den 27 juni 2021.