Tänk på följande kemiska jämvikt vid konstant temperatur:
3 timmar2 (g) + N2 (g) NH 2 NH3 (g)
Enligt Gay-Lussac är andelen volymer av gasformiga deltagare i en reaktion lika med förhållandet mellan respektive stökiometriska koefficienter. Enkelt sagt kan vi säga att antalet molekyler som finns i reaktanterna och produkterna är lika med koefficienterna i ekvationen.
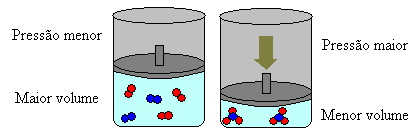
I ovanstående fall har vi i reagensen 4 molekyler och i produkterna har vi 2 molekyler, vilket innebär att volymen på reagensen är större och att produkten är mindre.
Om vi ökar trycket i detta system kommer balansen att flyttas mot den mindre volymen för att minska detta tryck. I fallet med den reaktion vi överväger kommer förskjutningen att ske i direkt riktning för produktbildning (NH3 (g)).
Men om vi sänker trycket kommer reaktionen att röra sig mot den största volymen, vilket är motsatt riktning, för bildning av reaktanter (3 H2 (g) + N2 (g)).
Sluta inte nu... Det finns mer efter reklam;)
Detta händer enligt Le Chateliers princip, som säger att störningar (som att minska eller öka trycket) orsakade i ett system i jämvikt kommer att få det att röra sig i den riktning som minimerar denna störning och justera sig själv till en ny balans.
I korthet kan vi säga följande när det gäller påverkan av tryckvariation på kemisk jämvikt:
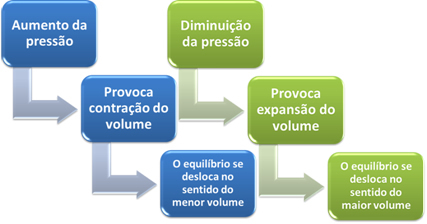
I fallet med reaktioner där volymen av reaktanterna är lika med volymen av produkterna ändras inte den kemiska jämvikten.
Av Jennifer Fogaça
Examen i kemi
Vill du hänvisa till texten i en skola eller ett akademiskt arbete? Se:
FOGAÇA, Jennifer Rocha Vargas. "Variation av tryck och förskjutning av kemisk balans"; Brasilien skola. Tillgänglig i: https://brasilescola.uol.com.br/quimica/variacao-pressao-deslocamento-equilibrio-quimico.htm. Åtkomst den 28 juni 2021.
Kemi

Testa dina kunskaper och lär dig mer med den här listan över lösta övningar om kemiska balanser. Genom detta material kommer du att kunna bättre förstå hur man bearbetar jämviktskonstanter (Kp, Kc och Ki), jämviktsförskjutning, pH och pOH, samt jämvikt i så kallade buffertlösningar.