Organiska föreningar kan representeras på olika sätt, såsom en platt strukturformel, en förenklad eller kondenserad strukturformel eller en streckformel. Den enklaste representationen är dock via molekylformeln.

Så låt oss se hur man bestämmer molekylformeln för organiska föreningar, baserat på de andra formlerna som nämns ovan.
1. Genom den platta strukturformeln:denna formel visar arrangemanget eller arrangemanget av atomer i molekylen. Till exempel nedan är den plana strukturformeln för en av de kolväten som finns i bensin.

Observera att i denna formel visas alla atomer och alla befintliga bindningar mellan dem. Nu, för att bestämma molekylformeln för denna förening, räkna bara antalet atomer för varje element och placera ett index på den nedre högra sidan av det aktuella elementet.
En viktig aspekt som ska belysas är att vi startar alltid molekylformeln för organiska föreningar från grundämnet kol, eftersom det är huvudbeståndsdelen i dessa ämnen. Se exemplet:
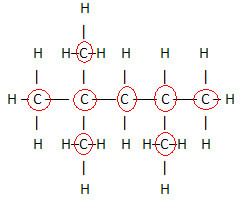
Eftersom det finns 8 kol, börjar vi skriva molekylformeln så här: Ç8
För att slutföra denna formel räknar vi mängden väten:
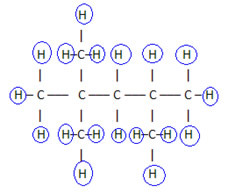
Så din molekylär formel é Ç8H18.
2. Genom den förenklade eller kondenserade strukturformeln: i denna typ av formel förkortas mängden väten. Titta till exempel på samma formel för molekylen som finns i bensin, nu i kondenserad form:
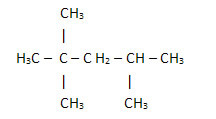
Sluta inte nu... Det finns mer efter reklam;)
På så sätt är det ännu enklare att räkna mängden väten, lägg bara till index (3 +3+ 3 +2 +1 +3 +3 = 18).
Men nu ska vi titta på den kondenserade strukturformeln för linolsyra, som finns i grönsaker som bomull, sojabönor, solrosor etc. och som används i färger och lacker:
H3C - CH2CH2CH2CH2CH═CH─CH2CH═CH─CH2CH2CH2CH2CH2CH2CH2─COOH
Räkna mängden kol, väte och oxygene har vi följande molekylär formel av linolsyra: Ç18H32O2.
3. Genom strokeformeln: denna formel förenklar ytterligare hur man representerar organiska föreningar, eftersom den utelämnar grupperna C, CH, CH2 och CH3.
Ett exempel är linolmolekylen, se hur den ser ut:

Låt oss först räkna mängden kol, och kom ihåg att i denna formel representeras varje bindning mellan kol. Således motsvarar spetsarna, liksom de två böjningspunkterna, kolatomer.
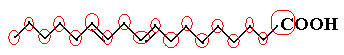
Så vi har: Ç18
För att räkna mängden väten måste vi komma ihåg att bindningarna mellan kol och väten är underförstådda, eftersom kol är känt för att göra fyra bindningar; sålunda är mängden bindningar som saknas mängden väte bunden till det elementet.
Se förklaringarna nedan:
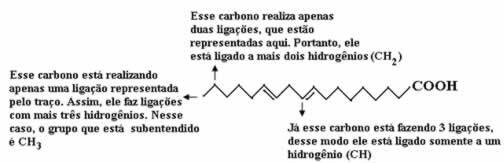
Således kommer mängden väten att vara: 32.

Mängden syre är ganska enkel att räkna, eftersom det bara finns två. Sedan molekylär formel é: Ç18H32O2.
Av Jennifer Fogaça
Examen i kemi
Vill du hänvisa till texten i en skola eller ett akademiskt arbete? Se:
FOGAÇA, Jennifer Rocha Vargas. "Molekylära formler av organiska föreningar"; Brasilien skola. Tillgänglig i: https://brasilescola.uol.com.br/quimica/formulas-moleculares-compostos-organicos.htm. Åtkomst den 28 juni 2021.
Kols rumsliga formel, Lewis elektroniska formel, planstruktur, elektroniska par, bindning kovalent, valenslager, utveckling av atommodellen, molekylformel, strukturformel, formler tredimensionell.
Kemiska formler, platt strukturformel, Couper strukturformel, trippelbindning, gas kväve, elektronisk formel, Lewis-formel, molekylformel, enkelbindning, dubbelbindning, gas kolsyra.



