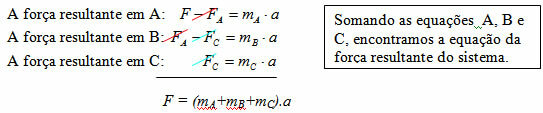När vi skickar in olika element till en flammas handling märker vi att var och en avger en annan färg. Om vi till exempel bränner ett strontium, ett natrium- och kopparsalt, kommer vi att se färgerna rött, intensivt gult och grönt, som visas i följande bild:

Om ljuset från dessa lågor faller på ett prisma, a diskontinuerligt spektrum, det vill säga endast några få färgade ljusa linjer kommer att observeras blandat med regioner utan ljus. För varje element kommer vi att ha ett annat spektrum.

Dessa typer av spektra kallas utsläppsspektrum, eftersom de utfärdades av ett visst element och tjänar till att identifiera det.
Det är möjligt att erhålla spektra som detta med hjälp av en ljusstråle som produceras i ett elektriskt urladdningsrör i hög temperaturer och lågt tryck, innehållande gaser från vissa element såsom väte, eller som ädelgaser vrål:

Genom att passera denna elektromagnetiska strålning (ljus) som produceras genom ett prisma, erhålls emissionsspektra för vart och ett av dessa element.
Tidigare trodde man att det uppnådda solspektrumet var helt kontinuerligt, men den engelska forskaren William Hyde Wollaston fann att arbeta med en mycket smal ljusstråle, med en slits på ca 0,01 mm, kunde du se att solspektret innehöll sju svarta linjer om det. Senare de unga Joseph Fraunhofer (1787-1826), med användning av prismer och diffraktionsgaller, fann att solspektrumet faktiskt innehåller tusentals överlagrade svarta linjer.
Någon tid senare den fysiska Gustav Robert Kirchhoff han märkte att de gula fläckarna, uppnådda med natriumspektrumet, befann sig på exakt samma plats som två svarta linjer i solens spektrum. han och kemisten Robert Wilhelm Bunsen genomförde flera experiment och märkte att om ett vitt ljus från Bunsen-brännaren, såsom solljus, passerade av det gula ljuset som emitterades av natrium och prisma korsades för att generera spektrumet; resultatet skulle vara ett kontinuerligt solspektrum, i regnbågens färger, men med de svarta linjerna (kallade D-linjerna från Fraunhofer) i samma position som de gula linjerna i natriumspektrumet.
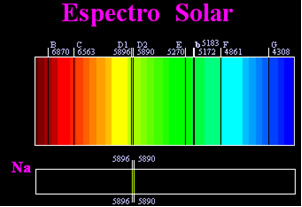
Solen avger ljus i alla färger, från rött till violett, men när de passerar genom jordens atmosfär absorberar de närvarande gaserna solens ljus exakt i de färger de avger.
Dessa typer av spektra kallas absorptionsspektra.
Baserat på dessa observationer, Kirchoff skapade tre lagar för spektroskopi, som är:
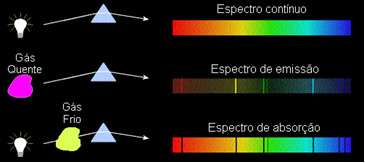
1) En kropp ogenomskinlig het, i något av de tre fysiska tillstånden, avger ett spektrum kontinuerlig.
2) En gas transparent - som de ädelgaser vi såg ovan - producerar en utsläppsspektrum, med utseendet på rader ljus. Antalet och positionen för dessa ledningar kommer att bestämmas av de kemiska elementen som finns i gasen.
3) Om a kontinuerligt spektrum passerar genom en gas vid den lägsta temperaturen, orsakar den kalla gasen närvaron av mörka linjer, det är en absorptionsspektrum. Detta är vad som hände med spektrumet av solljus som passerar genom natriumgasen. I detta fall beror antalet och positionen av ledningar i absorptionsspektrumet också på de kemiska elementen som finns i gasen.
Av Jennifer Fogaça
Examen i kemi
Källa: Brazil School - https://brasilescola.uol.com.br/quimica/espectros-emissao-absorcao-leis-kirchhoff.htm