Vi omges av utrustning som, för att fungera, behöver celler eller batterier. Men många av dessa bärbara enheter blir mindre och med det kommer det stora behovet av miniatyrbatterier.
Ett exempel på denna typ av batteri är kvicksilver eller kallas också kvicksilver-zinkhög.
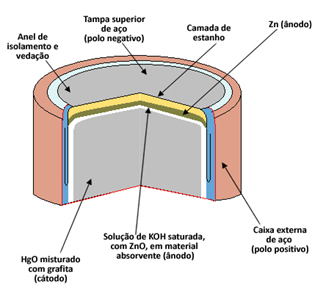
Varje cell består av två elektroder, anoden (negativ pol) och katoden (positiv pol) och en elektrolyt. När det gäller kvicksilvercellen, anod bildas av en kapsel av metalliskt zink (Zn(s)) det är katod per kvicksilveroxid II (HgO(s)). Både Zn och HgO males till pulver och komprimeras för att göra pålen så liten som möjligt. O elektrolyt är gjord av en lösning av mättad kaliumhydroxid (KOH(här)).
Zn oxiderar och donerar dess elektroner till HgO, vilket visas i halvreaktionerna och den globala reaktionen i denna cell nedan:
Anodhalvreaktion: Zn(s) + 2 OH1-(här) → ZnO(s) + 2 H2O(1) + 2e-
Katod halvreaktion: HgO(s) + H2O(1) + 2e- → Hg(1) + 2 OH1-(Deq)
Global reaktion: HgO(s) + Zn(s) → ZnO(s) + Hg(1)
Kvicksilverceller används i digitala klockor, armbandsur, kameror, miniräknare, elektroniska arrangörer, hörapparater och andra bärbara elektriska apparater som kräver effektivt arbete och hållbarhet, eftersom dessa batterier har spänning av 1,35V.

Tyvärr kan felaktigt avfallshantering av dessa batterier utgöra allvarliga risker för miljön eftersom de innehåller kvicksilver, som är en tungmetall. Kvicksilver kan förorena mark, grundvatten, sjö- och flodvatten och nå djur och människor. Det är giftigt även i små mängder. Bland de hälsoproblem som kvicksilver kan orsaka är: skador på slemhinnor, hud, njurar, våldsam illamående, kräkningar, buksmärtor, blodig diarré och det kan leda till döden.
För att ta reda på mer om varför batterier är giftigt avfall, hur kvicksilver är förorenat och vad vi ska göra med använda batterier, läs texterna nedan.
Av Jennifer Fogaça
Examen i kemi
Källa: Brazil School - https://brasilescola.uol.com.br/quimica/pilhas-mercurio.htm

