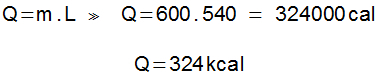Enligt den franska kemisten Henry Louis Le Chatelier, jämviktsförskjutning det är en situation där en kemisk reaktion förskjuts (framåt eller bakåt) när den utsätts för en yttre störning. Detta uttalande som kemisten föreslog blev känt som principen för Le Chatelier.
Notera: direkt reaktion är den i vilken reaktanterna omvandlas till produkter, medan den omvända reaktionen är den i vilken produkterna omvandlas till reaktanter.
En reaktion är i jämvikt när hastigheten för den direkta reaktionen är densamma som den omvända reaktionen, det vill säga reaktanter blir produkter i samma takt som produkter blir reaktanter.

Allmän representation av en kemisk jämviktsreaktion
Enligt Le Chateliers princip, när en kraft verkar på en jämviktsreaktion, jämviktsförskjutning det kommer att äga rum för att upphäva denna störning och upprätta en ny jämviktssituation i reaktionen.
De störningar som kan flytta en kemisk balans dom är:
→ koncentrationsvariation
när koncentration i materiens kvantitet (i mol / l eller molär) av en deltagare i reaktionen ändras (antingen minskat eller ökat),
balansförskjutning, så länge den deltagaren inte är i fast tillstånd.Således, enligt Le Chateliers princip, om koncentration om en deltagare ökas kommer balansen att flyttas i motsatt riktning till ökningen. Men om koncentration deltagaren minskar kommer det att ske en förskjutning av balansen i riktning mot minskningen. Till exempel:

Allmän representation av en kemisk jämviktsreaktion
Att öka koncentrationen av A = balans förskjuts åt höger
Minska koncentrationen av B = balansen förskjuts åt vänster
→ Variation av tryck
Tryckvariationen främjar bara jämviktsförskjutning som har gasformiga komponenter, eftersom molekylerna ökar kollisionerna med varandra när det ökas, och när trycket minskar minskar de kollisionerna med varandra.
Kollisionerna mellan molekyler ökar med ökande tryck, eftersom volymen (mellanslaget) minskas i enlighet därmed medan den minskar tryck åtföljs av ökande volym.
Sluta inte nu... Det finns mer efter reklam;)
Notera: I en kemisk jämvikt tar analysen av effekten av tryckmodifiering hänsyn till molvolymen av reaktanter och produkter, vilken volym är relaterad till reaktionskoefficienterna. I ekvationen nedan är reagensvolymen 4 och produkten är 2.
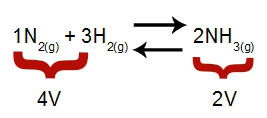
Ekvation som indikerar volymerna i ammoniakbildningen
Enligt Le Chateliers princip ökar förskjutningen av ett system om trycket i ett system ökas balans i riktning mot större volym, medan om trycket minskar, förskjutning av balans.

Ekvation som representerar balansen mellan ammoniakbildning
Ökande tryck = balans förskjuts åt höger (eftersom det är sidan med mindre volym).
Minskande tryck = balans förskjuts åt vänster (eftersom det här är den högre volymsidan).
→ Temperaturvariation
Ökningen i temperatur av en jämviktsreaktion gynnar molekylerna att kollidera mer, medan minskningen av temperatura minskar deras agitation och därmed deras chocker. Eftersom temperaturökningen alltid gynnar en reaktion endotermisk (en som absorberar energi).
Analysen av temperaturens effekt på en jämvikt tar huvudsakligen hänsyn till reaktionens ΔH. Om ΔH är positiv kommer den framåtriktade reaktionen att vara endoterm, medan den omvända kommer att vara exoterm. Om ΔH är negativ kommer den högra att vara exoterm och den inversa en endoterm.
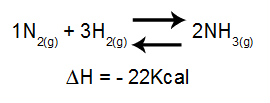
Ekvation som innehåller entalpi variation i ammoniakbildning
Ökande temperatur = jämvikt förskjuts åt vänster (eftersom detta är riktningen för den endotermiska reaktionen, eftersom Ah är negativ).
Minskande temperatur = jämvikt förskjuts åt höger (eftersom detta är riktningen för den exoterma reaktionen, eftersom Ah är negativ).
Av mig Diogo Lopes Dias
Vill du hänvisa till texten i ett skola eller akademiskt arbete? Se:
DAGAR, Diogo Lopes. "Vad är jämviktsförskjutning?"; Brasilien skola. Tillgänglig i: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-deslocamento-equilibrio.htm. Åtkomst den 28 juni 2021.