Ker obstajajo izjeme od pravila okteta, kako naj vemo pravilno razporeditev med atomi pri tvorbi molekule?
To lahko dosežemo z izračunom formalne obremenitve vsake konstrukcije. Formalni naboj, ki je najbližji nič, bo tisti z največjo verjetnostjo dejanskega obstoja. Upoštevajte, da je "najbližje ničli", zato ni nujno, da je nič.
Formula formalnega naboja (Cfo) é:
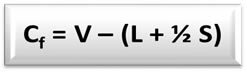
V = število valentnih elektronov prostega atoma;
L = število elektronov v izoliranih (nevezanih) parih atoma v strukturi;
S = število elektronov, ki jih ima atom v strukturi.
Da bi razumeli, kako se to zgodi, si predstavljajte, da želimo vedeti, kakšna je Lewisova elektronska struktura za molekulo SO.2. Obstajata dve možni ureditvi med atomi:
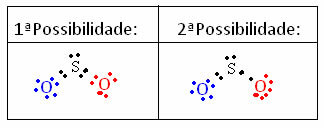
Izračuna se formalni naboj vseh atomov, ki sodelujejo v strukturah. Poglej:
1. možnost:
Žveplo (S): Kisik (O) Kisik (O)
Çf (S) = 6 – (2 + ½ 8) Çf (S) = 6 – (4 + ½ 4) Çf (S) = 6 – (4 + ½ 4)
Çf (S) =0 Çf (S) =0 Çf (S) =0
Ne ustavi se zdaj... Po oglaševanju je še več;)
2. možnost:
Žveplo (S): Kisik (O) Kisik (O)
Çf (S) = 6 – (2 + ½ 6) Çf (S) = 6 – (6 + ½ 2) Çf (S) = 6 – (4 + ½ 4)
Çf (S) = +1Çf (S) = -1 Çf (S) =0
Na podlagi dobljenih rezultatov lahko ugotovimo, da je 1. struktura tista z največjo verjetnostjo resničnega obstoja. Vemo torej, da ne sledi pravilu okteta, vendar je žveplo razširilo valentno lupino in ostalo stabilno z 10 elektroni.
To pravilo velja tudi za iskanje pravilne razporeditve ionov.
Avtorica Jennifer Fogaça
Diplomiral iz kemije
Bi se radi sklicevali na to besedilo v šolskem ali akademskem delu? Poglej:
FOGAÇA, Jennifer Rocha Vargas. "Izračun formalne obremenitve"; Brazilska šola. Na voljo v: https://brasilescola.uol.com.br/quimica/calculo-carga-formal.htm. Dostopno 28. junija 2021.

