Ko benzenski obroč že ima substituent, bo ta radikal vplival na vse druge substitucije H na obroču. Ta substituent je lahko orto in para-režiser ali meta-režiser. Toda porajajo se vprašanja:
| Kaj povzroči, da skupina, pritrjena na benzenski obroč, vpliva na smer in reaktivnost substitucijske reakcije? |
| Zakaj nekatere skupine ciljajo na svetovalce (onemogočanje), druge pa orto-para (aktiviranje)? |
Na ti dve vprašanji se odgovori z razumevanjem klicev. elektronski učinki da te skupine vadijo v ringu. Ta učinek se pojavi zaradi razlika elektronegativnosti med elementi, kot bo nadomestek polarizirajo vezi aromatičnega jedra, pri čemer izmenično inducirajo pozitiven značaj nekaterih obročastih ogljikov, medtem ko drugi ostanejo negativni.
| Nova zamenjava se bo zgodila v atomih ogljika, ki imajo značaj negativno. |
Poglejmo, kako se ti elektronski učinki pojavljajo v aromatskem obroču, pri čemer upoštevamo vrstni red elektronegativnosti elementov: F> O> N> Cl> Br> S> C> I> H.
1. primer: Radikalno aktiviranje ali orto-to-director:
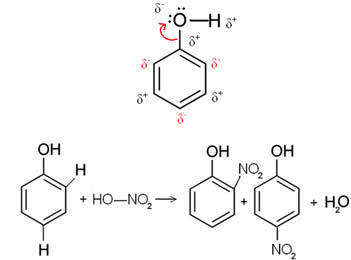
Na primer, v primeru pod molekulo benzola (fenola) je kisik najbolj elektronegativni element, torej pritegne k sebi elektrone, zaradi česar ima ogljik delno pozitiven naboj, ki inducira izmenična polarizacija obroča. Negativni položaji so natančno orto in para položaji. Zato skupina -OH je aktivirajoči radikal ali orto-režiserji. To je razvidno iz spodnje reakcije nitriranja fenola, ki kot produkta povzroča o-nitrofenol in p-nitrofenol:
Ne ustavi se zdaj... Po oglaševanju je še več;)
2. primer: deaktiviranje radikala ali meta-vodje:
Zdaj pa razmislite o primeru nitrobenzena:
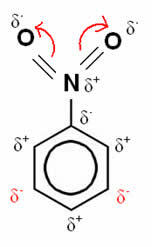
V tem primeru kisik ostaja najbolj elektronegativni element, zato privlači vezi z dušikom nase, ki je delno pozitivno naelektren, zaradi česar se na njega pritrjeni atom ogljika negativno polarizira in tako zaporedoma. Tako je položaj, ki postane negativen in najbolj dovzeten za zamenjavo, položaj cilj, ki je torej a onemogočanje.
Oglejte si zdaj podrobneje ta elektronski učinek, ki se imenuje resonančni učinek.
| resonančni učinek gre za privlačenje ali odbijanje elektronov na π (pi) vezi dvojnih ali trojnih vezi, ko odzvanjajo z samim benzenskim obročem. |
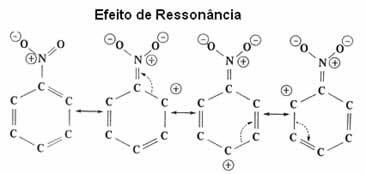
Kot je razvidno, skupina NO2 deaktivira obroč, saj mu jemlje elektrone in zmanjšuje elektronsko gostoto. Tako je skupina, ki bo napadla in izvedla zamenjavo (elektrofil) pozitivna, zato bo prednostno napadla meta položaj, ki je dobil negativni naboj.
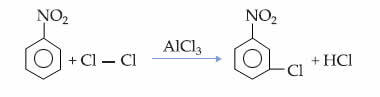
To je razvidno iz reakcije monokloriranja nitrobenzena, pri kateri pride do substitucije le v meta položaju:
Avtorica Jennifer Fogaça
Diplomiral iz kemije
Brazilska šolska ekipa
Bi se radi sklicevali na to besedilo v šolskem ali akademskem delu? Poglej:
FOGAÇA, Jennifer Rocha Vargas. "Elektronski učinki meta in orto-režiserjev radikalov"; Brazilska šola. Na voljo v: https://brasilescola.uol.com.br/quimica/efeitos-eletronicos-radicais-meta-orto-para-dirigentes.htm. Dostopno 28. junija 2021.