Joseph Lous Gay-Lussac (1778-1850) je bil znanstvenik, ki je opravil pomembne študije plinov. Izvedel je proizvodnjo vode iz reakcije med vodikovimi in kisikovimi plini in preveril, ali so vedno reagiral v razmerju med dvema količinama vodika in eno prostornino kisika, pri čemer je nastala dve prostornini Voda:
Vodik + kisik → Voda
1. poskus: 2 L 1 L 2 L
2. poskus: 4 L 2 L 4 L
3. poskus: 8 L 4 L 8 L
4. poskus: 16 L 8 L 160 L
Upoštevajte, da je v vseh poskusih razmerje vedno enako: 2: 1: 2.
Po več poskusih in analizah smo ugotovili, da se je enako zgodilo tudi pri drugih vrstah reakcij med plini, torej pri reakcijah vedno sledil konstantnemu količinskemu razmerju, je ta znanstvenik prišel do naslednjega zakona reakcij v plinastih količinah, znanega kot Volumetrični zakon Gay-Lussac ali Zakon o združitvi zvezkov:

Izjava volumetričnega zakona Gay-Lussaca
Toda ta zakon je bil proti Daltonova atomska teorija, ki je rekel, da so vse tvorili masivni in nedeljivi sferični delci, atomi. Po tej teoriji mora biti prostornina produktov v reakciji enaka vsoti količin reaktantov. Tako se mora zgoditi naslednje:
Vodik + kisik → Voda
2 zvezka + 1 zvezek → 3 zvezki
A Gay-Lussac je pokazal, da v praksi ni tako, rezultat je bil enak dvema količinama vodne pare.
Odgovor na to očitno protislovje je prišel skozi hipotezo ali Avogadrov zakon.

Znamka, natisnjena v Italiji, prikazuje Amedea Avogadra in napoved njegovega zakona leta 1956 *
Amedeo Avogadro (1776-1856) pokazali, da v resnici plini niso izolirani atomi, temveč molekule (z izjemo žlahtni plini). Njegov zakon je dejal:

Avogadrova pravna izjava
Avogadro je to pokazal 1 mol katerega koli plina ima 6.02. 1023 molekul. Ta vrednost je znana kot Avogadrovo število ali konstanta. Dokazano je bilo, da v normalnih pogojih temperature in tlaka (CNTP), pri katerih je tlak enak 1 atm in temperatura 273 K (0 ° C), prostornina, ki jo zavzame 1 mol katerega koli plina, bo vedno 22,4 L. Ta vrednost ustreza molska prostornina plinov. Ti odnosi so zelo pomembni za reševanje vaj stehiometrija.
To se morda zdi nenavadno, saj se lahko pojavi naslednje vprašanje: Kako lahko plini z molekulami in atomi različnih velikosti zasedajo enak volumen?
No, to je zato, ker so molekule plinov tako narazen, da je velikost molekul zanemarljiva.
Na ta način je Avogadrov volumetrični zakon razložil volumetrični zakon Gay-Lussaca. Spodaj upoštevajte, da dve molekuli vodika (dve prostornini) reagirata z eno molekulo kisika (en volumen) in tvorita dve molekuli vode (dve prostornini). Voda in vodik imata enak volumen, ker imata enako količino molekul, kot navaja Avogadrov zakon.
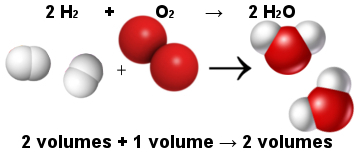
Delež med molekulami v reakciji tvorbe vode
Hkrati je Avogadrov zakon atomsko teorijo postavil v stališče, saj vidite, da je tako v reaktantih kot v produktih skupaj 6 atomov (4 vodik in 2 kisik).
Ti volumetrični zakoni so bili zelo pomembni za razvoj koncepta molekul.
* Zaščitena slika: rook76 / Shutterstock.com
Avtorica Jennifer Fogaça
Diplomiral iz kemije
Vir: Brazilska šola - https://brasilescola.uol.com.br/quimica/lei-volumetrica-gay-lussac.htm
