Atom ogljika je četverovalenten, to pomeni, da lahko tvori štiri kovalentne vezi, ki so lahko enojne, dvojne ali trojne. Poleg tega se te vezi lahko pojavijo z drugimi atomi ogljika ali z atomi drugih kemičnih elementov. Zahvaljujoč tej lastnosti ima ogljik edinstveno sposobnost, da nadaljuje s povezovanjem in oblikovanjem verig, ki so lahko kratke ali dolge.
Imenuje se ta sklop ogljikov, povezanih skupaj, in heteroatomov, ki tvorijo "okostje" organskih molekul ogljikove verige.
Ker je ogljik sposoben tvoriti zelo veliko število spojin, so bile te razvrščene glede na nekatere značilnosti svojih verig, da bi olajšali njihovo preučevanje in da bi jih bolje razumeli lastnosti.
Glavna razvrstitev teh spojin je:
1. Odprte ali aciklične verige: Ali so tisti, ki imajo dva ali več prostih koncev. Atomska veriga se ne zapre. Oglejte si nekaj primerov:
H3Ç? CH2? CH2? CH3 H3Ç? CH? CH? CH3 H3Ç? CH? CH3
?
CH3
2. Zaprte verige: So tisti, ki nimajo nobenih prostih koncev, saj se atomi povezujejo in tvorijo obroč ali cikel. Primeri:

Primeri zaprtih ogljikovih verig
Opazovanje: Odprte in zaprte verige, ki nimajo aromatičnega obroča (prva struktura spodnje vrstice na zgornji sliki), se imenujejo tudi aliciklike.
3. Mešane verige: So tisti, ki imajo vsaj en prosti konec in cikel, torej imajo vsaj en odprt in en zaprt del. Primeri:
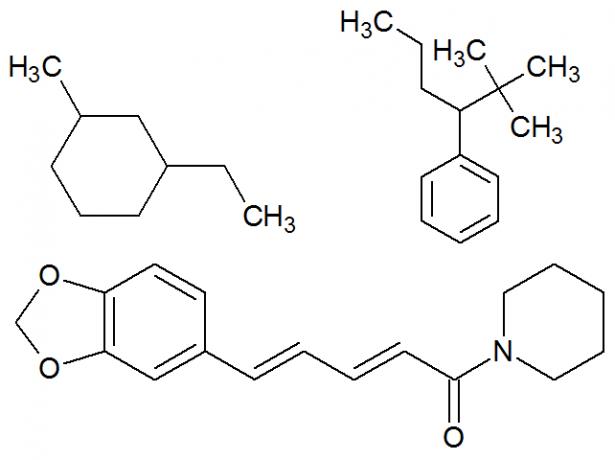
Primeri mešanih ogljikovih verig
Te tri glavne skupine so razvrščene tudi glede na druge podrazdelke, kot je prikazano na spodnjem diagramu:
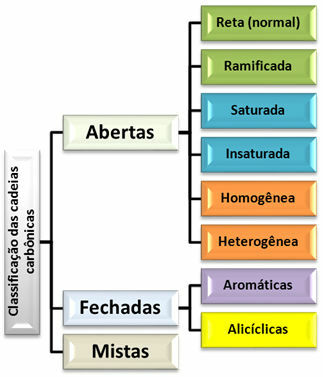
Shema razvrščanja ogljikovih verig
Če želite izvedeti več o vsaki od teh razvrstitev, preberite besedilo Klasifikacija ogljikovih verig, v oddelku Organska kemija.
Avtorica Jennifer Fogaça
Diplomiral iz kemije
Vir: Brazilska šola - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-classificacao-das-cadeias-carbonicas.htm