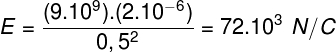Plinidealno je tista, kjer je trki med delci so popolnoma elastični. Med njegovimi delci ni kakršne koli interakcije sile privlačni ali odbijajoči, poleg tega ti delci ne zavzamejo prostora.
Glede na kinetična teorija plinov, termodinamično stanje idealnega plina v celoti opisujejo spremenljivke pritisk, prostornina in temperatura.
Poglejtudi: Kalorimetrija: miselni zemljevid, formule in rešene vaje
koncept idealnega plina
Idealni plini so sestavljeni izključno iz delcevvdimenzijetočen (zanemarljive velikosti), ki so v premikanjekaotično je vklopljen visokohitrost. Pri tej vrsti plina sta temperatura in hitrost prevajanja delcev sorazmerna.
Ker med delci idealnega plina ni medsebojne interakcije, notranja energija tega plina je vedno enaka vsoti kinetična energija vseh delcev, ki ga sestavljajo.
Ne glede na idealne pline bodo vedno enaki številkovdelcev za enako glasnost. Njihova masa pa bo neposredno odvisna od vaše molska masa
(izmerjeno v g / mol), poleg tega 1 mol idealnega plina (približno 6.0.1023 delci) bodo vedno zasedli a prostornina enaka 22,4 l.Ti pliniresnično, kjer obstaja pojav trkineelastična med delci se zelo približajo obnašanju idealnih plinov v režimi nizkega tlaka in visoke temperature. Po naključju je bila v normalnih pogojih tlaka in temperature na Zemlji (25 ° C in 1 atm) večina Plini se obnašajo kot idealni plini, kar olajša izračun napovedi o termodinamičnem vedenju njihovi.
Nekateri plini, kot je vodna para, ki je razredčena v atmosferski plin, ni mogoče šteti za idealne pline, ampak da pliniresnično. Ti plini imajo pomembne interakcije med delci, kar lahko zgosti, ki jih povzročajo utekočinjen, če obstaja padec temperature.
Ne ustavi se zdaj... Po oglaševanju je še več;)
Značilnosti idealnih plinov
Preverite na povzetek, nekaj značilnosti idealnih plinov:
- V njih se zgodijo le popolnoma elastični trki med delci;
- V njih med delci ni interakcij;
- V njih imajo delci zanemarljive dimenzije;
- 1 mol idealnega plina zavzame prostornino 22,4 l, ne glede na to, kateri plin je;
- Realni plini se obnašajo kot idealni plini, kadar so pod režimom nizkega tlaka in visoke temperature;
- Večina plinov se obnaša podobno kot idealni plini.
zakon o idealnem plinu
Preučevanje plinov, ki so jih razvili učenjaki Charlesboyle,JožefLouisgej-lussac in Robertboyle je privedlo do nastanka tri empirične zakone, ki se uporablja za razlago vedenja idealnih plinov v režimih temperatura, pritisk in glasnostkonstante, oz.
Ti zakoni so skupaj tvorili potrebno osnovo za nastanek zakon o idealnem plinu, ki se nanaša na začetno termodinamično stanje plina, opredeljeno s količinami P1, T1 in V1, S svojim končno termodinamično stanje (Str2, V2 in T2), potem ko je nekaj trpel transformacija plina.
Oglejte si formula splošnega zakona o plinu:
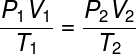
Splošni zakon o plinu določa, da izdelka daje pritisk krzno glasnostodplin, deljeno s termodinamično temperaturo, v kelvinah, je enako konstanti. To konstanto pa opisuje klapejronska enačba, pazi:
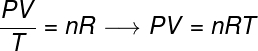
št - število molov (mol)
R - univerzalna konstanta popolnih plinov (0,082 atm.l / mol. K ali 8,31 J / mol. K)
V formuli: P je tlak, ki ga izvaja plin, V je prostornina, ki jo zavzema ta plin, in T je temperatura, izmerjena v kelvinah. veličino št se nanaša na število molov, medtem ko R je univerzalna konstanta idealnih plinov, ki se pogosto meri v enotah atm.l / mol. K ali v J / mol. K, slednjo je sprejela SI.
Poglejtudi:Kaj je sončni veter in kako vpliva na zemeljsko atmosfero?
Notranja energija idealnega plina
THE energijanotranje idealnih plinov lahko izračunamo z uporabo izdelka med konstantenvBoltzmann in termodinamične temperature, upoštevajte:
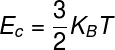
KB - Boltzmannova konstanta (KB = 1,38.10-23 J / K)
Iz prejšnjega razmerja, ki nam omogoča izračun povprečna kinetična energija iz delcev idealnega plina narišemo naslednjo formulo, po kateri lahko izračunamo, kakšna je povprečna kvadratna hitrost molekul idealnega plina za določeno temperaturo T upoštevajte:
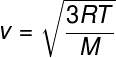
M - molska masa (g / mol)
Ta formula vam omogoča, da vidite, da a poleg tegaobtemperatura idealnega plina povzroči povečanje srednje kvadratne hitrosti delcev.
Izvedite več:Ugotovite, iz česa je sestavljena svetloba in kakšne so njene značilnosti
Rešene vaje na idealnih plinih
Vprašanje 1) Dva mola idealnega plina in pod tlakom 1 atm najdemo pri temperaturi 227 ° C. Izračunajte prostornino tega plina v litrih.
Podatki: R = 0,082 atm.l / mol. K
a) 75 l
b) 82 l
c) 15 l
d) 27 l
e) 25 l
Predloga: Črka B
Resolucija:
Za izračun prostornine tega plina bomo uporabili Clapeyronovo enačbo, vendar preden moramo opraviti izračun, moramo temperaturo 227 ° C pretvoriti v kelvin. Za to tej temperaturi dodamo faktor 273, kar ima za posledico temperaturo 500 K.
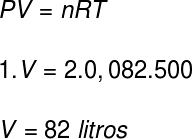
Glede na ločljivost znaša prostornina plina 82 litrov.
Vprašanje 2) Idealen plin zasede prostornino 20 l, ko je pod pritiskom 3 atm, tako da njegova temperatura ostane konstantna, njegova prostornina pa se potroji. Izračunajte končni tlak tega plina po prehodu.
a) 1 atm
b) 3 atm
c) 5 atm
d) 8 atm
e) 9 atm
Predloga: Črka a
Resolucija:
Za rešitev te naloge bomo uporabili splošni zakon o plinih, upoštevajte:
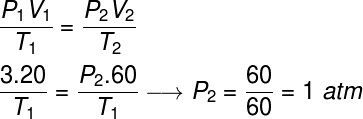
Za izračun je bilo treba plinu dodeliti prostornino 60 l, saj se je njegova količina med preoblikovanjem potrojila.
Avtor Rafael Hellerbrock
Učitelj fizike