Fuzija je prehod iz trdnega v tekoče stanje. Pojavi se, ko telo, ki je pod določenim pritiskom, prejme toploto in njegova temperatura doseže določeno vrednost.
Količina toplote, ki jo mora telo prejeti, da postane popolnoma tekoče, je odvisna od snovi, ki jo sestavlja.
Na splošno ima snov v trdnem stanju natančno določeno obliko. Njeni atomi so lepo razporejeni v strukturo, imenovano a kristalno omrežje.
Ko prejme toploto, atomi, ki tvorijo trdno snov, povečajo svoje vibracije in povečajo svojo temperaturo.
Če se dohodna energija poveča, bodo vibracije atomov prekinile kristalno mrežo in telo bo prešlo v tekoče stanje.

Zakoni o združitvah
- Ob ohranjanju konstantnega tlaka ostane temperatura med postopkom taljenja konstantna.
- Količina toplote na masno enoto se imenuje latentna toplota fuzije in je značilnost snovi.
- Temperatura, pri kateri se vsaka snov topi, je dobro določena in se imenuje fuzijska točka.
Ko je pod pritiskom 1 atmosfere, se voda stopi pri 0 ° C, medtem ko je tališče železa 1,535 ° C in klora 101,5 ° C.
Količina latentne toplote
Količina toplote, ki jo telo potrebuje za spremembo stanja, je odvisna od vrednosti latentna toplota fuzije in mase telesa.
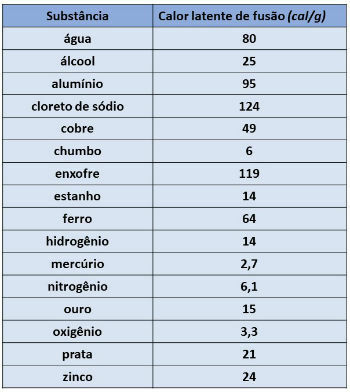
Vrednost latentne toplote se razlikuje glede na snov, ki sestavlja telo. V spodnji tabeli predstavljamo vrednosti nekaterih snovi.
Formula
Količina toplote, ki jo telo potrebuje za spremembo faze, je podana s formulo:
Biti,
V: količina latentne toplote (apno)
m: masa (g)
Lf: latentna toplota fuzije (kal / g)
Upoštevajte, da formula za količino toplote pri fazni spremembi ne upošteva temperaturnih sprememb.
To je zato, ker se celotna količina prejete toplote porabi za razbijanje kristalne rešetke, pri čemer je temperatura ves čas postopka konstantna.
Primer
Koliko toplote je potrebno za popolno zlitje bloka zlata z maso 200 g?
Latentna toplota fuzije zlata je enaka 15 kal / g (tabela zgoraj), zato bomo imeli:
Q = 200. 15 = 3000 kal ali 3 kcal
Če želite izvedeti več, preberite tudi:
- Spremembe fizičnega stanja
- Fizična stanja snovi
- Fizična stanja vode
- Lastnosti snovi
- Diagram faz
- Utekočinjenje ali kondenzacija
- Vreti
- Izhlapevanje
- Sublimacija
- Utrjevanje
- Elektroliza
- Izhlapevanje