V reakcije dodajanjav alkeni(ogljikovodiki, ki imajo dvojno vez med dvema atomoma ogljika), pi vez med dvema ogljikoma se pretrga in vsak ogljik se veže na nov atom. Poglej:
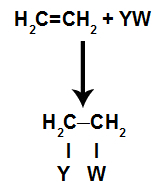
Splošni shematski model adicijske reakcije
Načela adicijske reakcije
a) Prekinitev povezave pi
Pi vez se zlahka pretrga, ker je šibkejša kot sigma vez. Da pa se to lahko zgodi, je potrebno, da je alken podvržen pogojem, ki zagotavljajo to motnjo. Po prekinitvi vezi pi med dvema ogljikoma se na vsakem od vključenih ogljikov vedno pojavi vezno mesto (za nove atome).
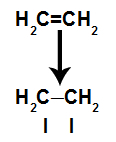
Shema, ki prikazuje prekinitev povezave pi
b) Pogoji za prekinitev pi vezi
Dejavniki, ki podpirajo prekinitev vezi pi, so:
Uporaba katalizatorjev;
Ogrevanje;
Prisotnost kisline v reakcijskem mediju.
c) Pojav adicijske reakcije
Vezna mesta, ki nastanejo po prekinitvi pi-vezi, bodo vedno zasedala atomi reaktanta, ki je v isti posodi kot alken. Reakcija dodajanja je poimenovana po vrsti reagenta, pomešanega z alkenom.
Vrste adicijskih reakcij v Alkenih
a) Hidrogeniranje
Alken zmešamo s plinom vodika (H
2) v posodi in izpostavljen trdnemu katalizatorju (nikelj, platina ali paladij) in ogrevanju (Δ).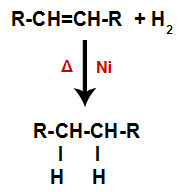
Splošna shema reakcije hidrogeniranja v alkenih
Prisotnost katalizatorja in ogrevanje povzročata pi vez alkena in sigma vez med vodikoma H2 se hitreje zlomijo. S tem smo ustvarili dve vezni mesti v alkenu in dva prosta atoma vodika v reakcijskem mediju.

Ustvarjanje mest vezave in ločevanja atomov
Tako takoj zatem vsak prosti atom vodika zavzame eno od veznih mest, nastalih v alkenu. Ker ima nastala snov le ogljike in vodike, pa tudi le preproste vezi med ogljiki, je a alkan.
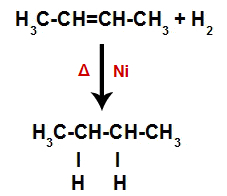
Enačba, ki predstavlja tvorbo alkana pri hidrogeniranju
B) Halogeniranje
Alken se meša s preprostimi snovmi (F2, Cl2, br2 zdravo2), ki ga tvori halogeni (klor, fluor, jod in brom) v posodi in izpostavljen delovanju svetlobe (λ) in segrevanju (Δ).

Splošna shema reakcije halogeniranja v alkenih
Delovanje svetlobe in segrevanja omogoča hitrejšo prekinitev pi-vezi alkena in sigma-vezi med snovmi, ki jih tvori halogen. S tem imamo v reakcijskem mediju dve alkenski vezi in dva prosta atoma halogena.

Ustvarjanje mest vezave in ločevanja atomov
Tako takoj zatem vsak prosti atom halogena zavzame eno od veznih mest, ki nastanejo v alkenu. Ker ima nastala snov halogen, povezan s strukturo, sestavljeno iz ogljikov in vodikov, je a organski halid.

Enačba, ki predstavlja tvorbo organskih halidov pri halogeniranju
c) Hidracija
Alken zmešamo z vodo (H2O) v posodi in podvržen delovanju katalizatorja (v tem primeru žveplove kisline).
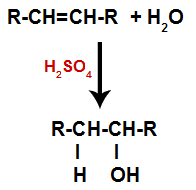
Splošna shema reakcije hidracije v alkenih
Prisotnost žveplove kisline v reakciji hitreje pretrga pi vez alkena in sigma vez med vodikom (H) in hidroksilom (OH) vode. S tem smo ustvarili dve vezavni mesti v alkenu ter prosti vodik in hidroksil v reakcijskem mediju.
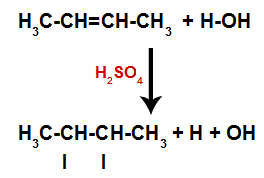
Ustvarjanje mest vezave in ločevanja atomov
Tako kmalu zatem vodik in hidroksil zasedeta eno od veznih mest, ki nastaneta v alkenu. Ker se tvorjena snov hidroksilno veže na nasičen ogljik (tvori le preproste vezi), je alkohol.
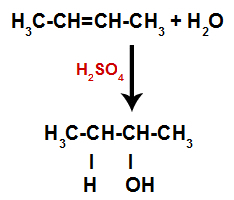
Enačba, ki predstavlja tvorbo alkohola pri hidraciji
d) Dodajanje vodikov halogenidi
Alken v posodi zmešamo s halogenirano anorgansko kislino (HF, HI, HCl, HBr).

Splošna shema reakcije kislinskega halida v alkenih
Prisotnost kisline v reakciji povzroči hitrejšo prekinitev vezi pi alkena. Enotna vez v kislini je prekinjena, ker se te snovi naravno ionizirajo. Tako se v alkenu ustvarita dve vezavni mesti, v reakcijskem mediju pa sta prosti vodik in halogen.
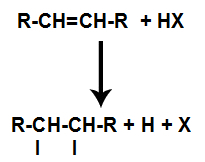
Ustvarjanje mest vezave in ločevanja atomov
Tako kmalu zatem vodik in halogen zasedeta eno od veznih mest, ki nastaneta v alkenu. Ker ima nastala snov halogen, povezan s strukturo, sestavljeno iz ogljikov in vodikov, je organski halid.
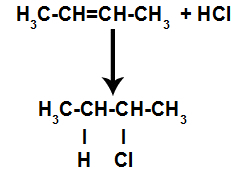
Enačba, ki predstavlja tvorbo organskih halidov pri halogeniranju
Jaz, Diogo Lopes Dias
Vir: Brazilska šola - https://brasilescola.uol.com.br/quimica/reacoes-adicao-alcenos.htm

