Za družine periodnega sistema so navpična zaporedja mize in zbirajo kemični elementi s podobnimi kemičnimi lastnostmi. Takšne podobnosti so posledica prisotnosti enakih količin valenčnih elektronov za elemente, združene v isto družino. Družine sprejmejo reprezentativne elemente v skupinah 1 in 2, od 13 do 18 in prehodne elemente v skupinah 1 do 12.
Preberite tudi:Transuranski elementi — kemični elementi, ki jih je ustvaril človek in so v periodnem sistemu za uranom
Povzetek družin periodnega sistema
Družine ustrezajo navpičnim linijam Periodni sistem.
Družine v periodnem sistemu, znane tudi kot skupine, so oštevilčene od 1 do 18.
Kemijski elementi v isti družini imajo podobne kemijske lastnosti.
Poznavanje niza elementov je razloženo z enakim številom valenčnih elektronov.
Reprezentativni elementi so razdeljeni v skupine 1, 2, 13, 14, 15, 16, 17 in 18. Vsaka od teh družin ima posebna imena.
Prehodni elementi tvorijo eno samo družino, ki je razdeljena v skupine 3, 4, 5, 6, 7, 8, 9, 10, 11 in 12.
Organizacija družin periodnega sistema
Družine v periodnem sistemu so navpična zaporedja tabele, torej stolpce. Znane tudi kot skupine, družine periodnega sistema so oštevilčene od 1 do 18, od leve proti desni.
Za kemijske elemente, ki zasedajo isti stolpec, velja, da so v isti družini., zaradi podobnosti med njunimi kemijskimi lastnostmi, ki je posledica dejstva, da imata enako število elektroni pri valenčna lupina. Na primer, vsi kemični elementi družine 18 imajo osem elektronov v valenčni lupini (polna lupina) in le redko sodelujejo pri kemične vezi.
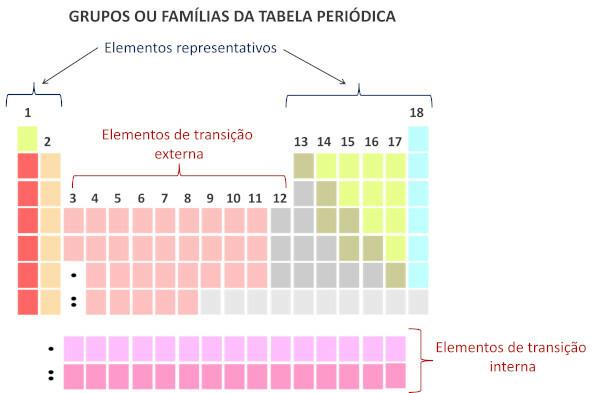
Po sodobnem sistemu Mednarodna zveza za čisto in uporabno kemijo (Iupac) je vsaka skupina ali družina označena s številko od 1 do 18, začenši od leve proti desni v periodnem sistemu.
Pomembno je poudariti, da je stari sistem IUPAC sprejel alfanumerični sistem, s črkama A in B za reprezentativne in prehodne elemente. Trenutno se ta vrsta nomenklature ne uporablja več.
Nomenklatura družin periodnega sistema
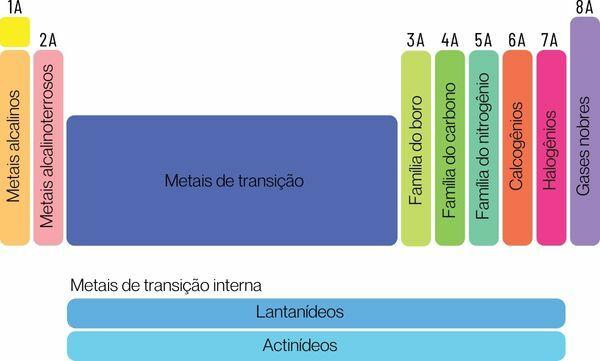
Kemijske elemente lahko razvrstimo v dve veliki družini: reprezentativne elemente in prehodne elemente.
→ Reprezentativni elementi periodnega sistema
Reprezentativni elementi so razdeljeni v skupine 1, 2, 13, 14, 15, 16, 17 in 18. Vsaka od teh skupin ima določeno ime, po katerem je lahko tudi znana. poglej:
Skupina 1: družina kovine alkalno.
2. skupina: družina zemeljsko alkalijske kovine.
Skupina 13: bor ali družina zemeljskih kovin.
Skupina 14: družina ogljika.
Skupina 15: Družina dušika ali pnikogenov.
Skupina 16: družina kisika ali halkogena.
Skupina 17: družina halogeni.
Skupina 18: družina žlahtni plini.
→ Prehodni elementi periodnega sistema
Ti prehodni elementitvorijo eno družino, razdeljeno v skupine 3, 4, 5, 6, 7, 8, 9, 10, 11 in 12. Serije lantanoidov in aktinidov so prav tako del prehodnih elementov.
Prehodni elementi vsi so kovinski in imajo podobne kemijske lastnosti, čeprav imajo različne elektrone v valenčni lupini in bi zato tvorili eno samo in veliko družino prehodnih kovin.
Kemijski elementi iz družin periodnega sistema
Vsaka družina ali skupina je sestavljena iz niza kemičnih elementov. Oglejte si opis kemijskih elementov, ki sestavljajo vsako družino:
Skupina 1:litij, natrij, kalij, rubidij, cezij, francij.
2. skupina:berilij, magnezij, kalcij, stroncij, barij, radio.
Skupina 3:skandij, itrij, serije lantanidov in serije aktinidov.
Skupina 4: titan, cirkonijO, hafnij je rutherfordij.
Skupina 5:vanadij, niobij, tantal je dubnij.
Skupina 6:krom, molibden, volfram je seaborgium.
Skupina 7:mangan, tehnecij, renij je bohrio.
Skupina 8: železo, rutenij, osmij je hasij.
Skupina 9:kobalt, rodij, iridij in meitnerij.
Skupina 10:nikelj, paladij, platina in darmstadtio.
Skupina 11: baker, srebro, zlato in rentgenij.
Skupina 12:cink, kadmij, Merkur in Kopernik.
Skupina 13: bor, aluminij, galij, indij in talij.
Skupina 14: ogljik, silicij, germanij, kositer, svinec in flerovium.
Skupina 15:dušik, fosfor, arzen, antimon je bizmut.
Skupina 16:kisik, žveplo, selen, telur, polonij in livermorij.
Skupina 17: fluor, klor, brom, jod in astatin.
Skupina 18:helij, neon, argon, kripton, ksenon je radon.
Pomembno: kemični element vodik je poseben primer, ker kljub temu, da se nahaja poleg skupine 1, ni del družine alkalijskih kovin, saj nima podobnih kemijskih lastnosti.
Izvedite več: Kateri so radioaktivni elementi v periodnem sistemu?
Glavne značilnosti družin periodnega sistema
→ Skupina 1 ali družina alkalijskih kovin
So kovinske trdne snovi, sijoče in gladke.
Imajo visoko toplotno prevodnost in visoko Električna prevodnost.
imajo temperature relativno nizko tališče.
So zelo reaktivni z vodo.
Nagnjenost k tvorbi enovalentnih kationov (naboj +1).
→ Skupina 2 ali družina zemeljskoalkalijskih kovin
So kovinske trdne snovi, sijoče in trše v primerjavi z alkalnimi kovinami.
Z lahkoto oksidirajo.
Imajo visoko toplotno prevodnost in visoko električno prevodnost.
V primerjavi z alkalijskimi kovinami imajo nekoliko višje temperature taljenja.
Reaktivni so z vodo.
Nagnjenost k tvorbi dvovalentnih kationov (naboj +2).
→ Skupine 3 do 12 ali družina prehodnih kovin
So največja družina v periodnem sistemu.
Trde, sijoče kovinske trdne snovi.
Imajo visoko toplotno prevodnost in visoko električno prevodnost.
Gosto.
Visoke temperature taljenja.
se lahko predstavlja drugače oksidacijska stanja.
→ Skupina 13 ali borova družina
Imajo vmesne lastnosti med lastnostmi kovin in ne kovine.
V okoljskih pogojih so trdni.
Nagnjenost k tvorbi trivalentnih kationov (naboj +3).
→ Skupina 14 ali družina ogljika
Imajo vmesne lastnosti med lastnostmi kovin in nekovin.
V okoljskih pogojih so trdni.
Nagnjenost k oblikovanju štirih vezi.
V okoljskih pogojih so trdni.
Ogljik in silicij lahko tvorita verižne vezi.
→ Skupina 15 ali družina dušika
Imajo vmesne lastnosti med lastnostmi kovin in nekovin.
Trdne snovi pri sobnih pogojih, z izjemo dušika, ki je plin.
Dušik in fosfor sta temeljna v živih organizmih.
Arzen je zelo strupen.
→ Skupina 16 ali družina kisika (halkogeni)
Imajo različne lastnosti, ki se spreminjajo od nekovinskega do kovinskega elementa, ko greste navzdol po družini.
Trdne snovi pri sobnih pogojih, z izjemo kisika, ki je plin.
Nagnjenost k tvorbi dvovalentnih anionov (naboj -2).
→ Skupina 17 ali družina halogenov
So nekovine.
Precej reaktivno.
Slabi toplotni in električni prevodniki.
V okoljskih pogojih obstajata fluor in klor kot plini, brom je tekoč, jod pa trdna snov.
Nagnjenost k tvorbi enovalentnih anionov (naboj -1).
→ Skupina 18 ali družina žlahtnih plinov
So nekovine.
Zelo malo reaktivni, zato jih lahko imenujemo inertni plini.
Obstajajo v obliki plinov.
Nimajo nagnjenosti k oblikovanju ioni.
Periodni sistem in elektronska distribucija
Kemični elementi, ki pripadajo isti družini ali skupini, imajo podobne kemijske lastnosti, ker jih imajo enako število elektronov v valenčni lupini.
Število elektronov v valenčni lupini je relevantno, saj določa težnjo po nastanku kationov oz anioni, vrsta kemične vezi, ki se tvori, energija, vključena v kemične reakcije, med drugim značilnosti. Da bi našli število valenčnih elektronov, je treba poznati atomsko število elementa in izvedite svoje elektronska distribucija.
→ Elektronska distribucija reprezentativnih elementov
Reprezentativni elementi imajo najbolj energijske elektrone v podnivojih s je p elektronske plasti (n). Naslednja tabela združuje elektronske konfiguracije, povezane z vsako družino reprezentativnih elementov. izraz n spreminja od 1 do 7 in predstavlja raven energije, ki jo zasedajo valenčni elektroni, kar je enako periodi (vodoravni črti) periodnega sistema, v katerem je element.
Elektronska distribucija reprezentativnih elementov | ||
družina ali skupina |
Elektronska distribucija |
Primer |
1 |
nas1 |
Li (Z=3): 1s2 2s1 |
2 |
nas2 |
Be (Z=4): 1s2 2s2 |
13 |
nas2 np1 |
B (Z=5): 1s2 2s22p1 |
14 |
nas2 np2 |
C (Z=6): 1s2 2s22p2 |
15 |
nas2 np3 |
N (Z=7): 1s2 2s22p3 |
16 |
nas2 np4 |
O (Z=8): 1s2 2s22p4 |
17 |
nas2 np5 |
F (Z=9): 1s2 2s22p5 |
18 |
nas2 np6 |
Ne (Z=10): 1s2 2s22p6 |
→ Elektronska razdelitev prehodnih elementov
Prehodni elementi so razporejeni med skupinama 3 in 12 ter imajo podravni d je f zasedajo valenčni elektroni:
Zunanji prehodni elementi: zadrži valenčne elektrone v podravni d, pri čemer je elektronska konfiguracija enaka nas2 (n-1)d(1 do 8). Na primer, element nikelj (Z = 28) spada v skupino 10, njegova konfiguracija pa je 1s2 2s2 2p6 3s2 3p6 4s2 3d8.
Notranji prehodni elementi: so del skupine 3, vendar so "notranji" periodnega sistema in so razširjeni pod njim v obdobjih 6 (lantanidi) in 7 (aktinidi). Ti elementi imajo valenčne elektrone, ki zasedajo podlupino f in splošno elektronsko konfiguracijo nas2 (n-2)f(1 do 13). Na primer, element lantan (Z = 57) je prvi element v seriji lantanidov, njegova elektronska konfiguracija pa je 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f1.
Vedite tudi:Kakšen je izvor periodnega sistema?
Rešene vaje o družinah periodnega sistema
Vprašanje 1
(UFC — prilagojeno) Glede sodobne periodične klasifikacije elementov označite pravilno trditev:
A) V periodnem sistemu družine ali skupine ustrezajo vodoravnim črtam.
B) Elementi v družini imajo zelo različne kemijske lastnosti.
C) V družini imajo elementi na splošno enako število elektronov v zadnji lupini.
D) V obdobju imajo elementi podobne kemijske lastnosti.
E) Reprezentativni elementi so razdeljeni v skupine od 3 do 12.
Resolucija:
Alternativa C
Točka A je napačna: družine ali skupine so stolpci (navpične črte) periodnega sistema.
Točki B in D sta napačni: V družini imajo elementi podobne kemijske lastnosti. V obdobjih imajo elementi enako elektronsko lupino, ki jo zasedajo valenčni elektroni.
Točka C pravilno: V družini imajo elementi enako število elektronov v zadnji lupini.
Točka E ni pravilna: reprezentativni elementi so skupine 1, 2, 13, 14, 15, 16, 17 in 18. Prehodni elementi so razdeljeni v skupine od 3 do 12.
vprašanje 2
(EAM) Elementi A, B in C imajo v svojih valenčnih lupinah naslednje elektronske konfiguracije:
A: 3s1
B: 4s2 4p4
C: 3s2
Na podlagi teh podatkov izberite pravo možnost.
A) Element A je alkalijska kovina.
B) Element B je halogen.
C) Element C je halkogen.
D) Elementa A in B pripadata tretji periodi periodnega sistema.
E) Trije elementi spadajo v isto skupino periodnega sistema.
Resolucija:
Alternativa A
Točka A pravilna: element A ima elektronsko porazdelitev, ki vsebuje samo en valenčni elektron, zato spada v 1. skupino periodnega sistema.
Napačen element B: element B ima konfiguracijo elektronov 4s2 4p4, kar pomeni, da je v zadnji lupini 6 elektronov in da ta element spada v skupino 16 (halkogeni).
Nepravilen element C: element C ima elektronsko konfiguracijo z 2 elektronoma v zadnji lupini, zato je element skupine 2 v tabeli.
Napačna postavka D: element A spada v tretjo periodo (n = 3), element B pa v četrto periodo (n = 4).
Napačen element E: trije elementi imajo različne količine elektronov v zadnji lupini, zato ne morejo biti del iste družine.
Avtor: Ana Luiza Lorenzen Lima
Učiteljica kemije
Vir: Brazilska šola - https://brasilescola.uol.com.br/quimica/familias-da-tabela-periodica.htm

