Za kisikova funkcija so skupina organske spojine ki imajo atome kisika vezane na ogljikovo verigo. Ali so:
alkohol;
keton;
aldehid;
karboksilna kislina;
ester;
eter.
Preberite tudi:Ogljikovodiki - spojine, sestavljene iz ogljika in vodika
Povzetek o delovanju kisika
Kisikove funkcije so skupina spojin, ki vsebujejo atom kisika. kisik pritrjen neposredno na ogljikovo verigo.
Za različne kisikove funkcije je značilna posebna strukturna ureditev atomi, ki se imenuje funkcionalna skupina.
Funkcionalne skupine so odgovorne za lastnosti vsake organske funkcije.
Kisikove funkcije so: alkohol, keton, aldehid, karboksilna kislina, ester in eter.
Video lekcija o delovanju kisika
Kakšne so funkcije kisika?
Telesne funkcije s kisikom so tiste, ki imajo atom kisika vezan na atom kisika ogljik ogljikove verige.
Funkcije kisika so:
alkohol;
keton;
aldehid;
karboksilna kislina;
ester;
eter.
Organske funkcije prepoznajo po svoji funkcionalni skupini, ki je strukturna razporeditev atomov ali vezi, odgovorna za značilne lastnosti te skupine spojin.
Pomen kisikovih funkcij
Prisotnost kisika deluje v organskih spojinah lahko spremeni lastnosti spojin, v primerjavi z ustreznim ogljikovodikom, z enakim številom ogljikov.
Za kisikove funkcije je značilna prisotnost hidroksilnih, karbonilnih ali karboksilnih skupin. A prisotnost atoma kisika poveča polarni značaj spojine, zaradi česar postanejo bolj hidrofilne, to je poveča njihova afiniteta za vodo.
Pojav kisikovih funkcij je odgovoren tudi za vrsto medmolekularna silaki deluje med molekulami. Narava in intenzivnost medmolekulskih sil vplivata na topnost ter temperature taljenja in vrelišča.
Spodnja tabela prinaša primerjavo med nekaterimi lastnostmi treh spojin, ki imajo enako število ogljikovih atomov, razlikujejo pa se po prisotnosti kisikovih funkcionalnih skupin.
Organski kompost | |||
Butan (C4H10) |
Butanon (C4H8O) |
Butanol (C4H10O) |
|
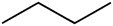 |
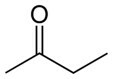 |
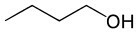 |
|
organsko funkcijo |
Ogljikovodik |
keton (funkcija kisika) |
Alkohol (funkcija kisika) |
Polarnost |
nepolaren |
Polar |
Polar |
temperatura taljenja |
-138,3 °C |
-86°C |
-89°C |
temperatura vrelišča |
-0,5°C |
80°C |
118°C |
Prevladujoča medmolekularna sila |
Inducirani dipol |
stalni dipol |
vodikove vezi |
Alkohol
Alkohol z organsko funkcijo ima hidroksilno skupino (-OH), vezano neposredno na nasičen ogljik, to je tisti ogljikov atom, ki vzpostavlja samo enojne vezi.
Funkcionalna skupina alkoholov: R-OH (hidroksil).
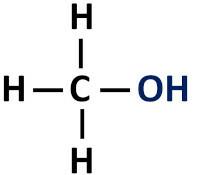
alkoholi so razvrščeni glede na vrsto ogljika, na katerega je vezan hidroksil. Primarni alkoholi imajo hidroksil vezan na primarni ogljik. Sekundarni alkoholi imajo hidroksilno skupino vezano na sekundarni ogljik, terciarni alkoholi pa svojo -OH skupino vezano na terciarne ogljike.
Organska spojina, ki ima samo en hidroksil, se imenuje monoalkohol. Če ima dve hidroksilni skupini, se imenuje dialkohol. Nad tem se molekule imenujejo polialkoholi.
A nomenklatura za alkohole sledi priporočilu Iupac (Mednarodna zveza za čisto in uporabno kemijo), pri čemer upošteva sestavo imena kemijskih struktur v treh delih:
Predpona – povezana s številom ogljikov.
Infiks – se nanaša na vrsto kemične vezi, vzpostavljene med ogljikovimi atomi.
Pripona – povezana s funkcijsko skupino. V primeru alkoholov je uporabljena pripona -zdravo.
Oglejte si primere:
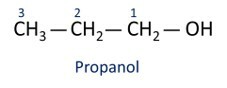
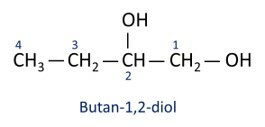
O glavni alkohol je etanl (CH3CH2OH), ki se uporablja kot gorivo, v alkoholnih pijačah, kot kemično topilo, čistilno sredstvo in razkužilo.
keton
Funkcija organskega ketona ustreza karbonilna funkcionalna skupina (C=O), ki se nahaja med dvema atomoma ogljika ogljikove verige.
Funkcionalna skupina ketonov: R1–(C=O)–R2.

Ketoni so razvrščeni glede na število karbonilnih skupin:
Monoketoni – imajo eno karbonilno skupino.
Diketoni – imajo dve karbonilni skupini.
Politoni – imajo več kot dve karbonilni skupini.
A nomenklatura za ketone sledi pravilom Iupac, vendar z razliko v črkovanju pripone. Ketone prepoznamo po priponi -ona.
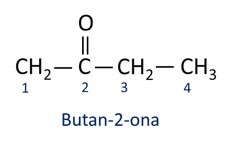
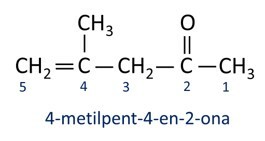
Na splošno se ketoni uporabljajo v proizvodnji drugih kemikalij in farmacevtskih izdelkov. V industriji se ketoni uporabljajo kot topila za barve, barvila in lake. Eden najbolj znanih ketonov je propanon, ki je v javnosti znan kot aceton. Raztopine acetona se uporabljajo za odstranjevanje laka za nohte.
Preberite tudi:Amidi - spojine, ki imajo dušik vezan na karbonil
Aldehid
Funkcija organskega aldehida je označen s prisotnostjo karbonilne funkcionalne skupine, katerega ogljikov atom ima vodikovo vez.
Funkcionalna skupina aldehidov: H–C=O (formil).
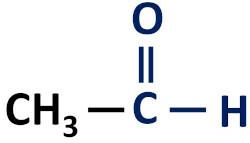
Aldehidi se vedno pojavijo na koncu ogljikovih verig, ker mora biti njihov ogljikov atom vezan na vsaj en atom vodika.
A nomenklatura za aldehidne spojine sledi pravilom IUPAC, razlikuje se po končnici. Aldehide prepoznamo s pripono -al.
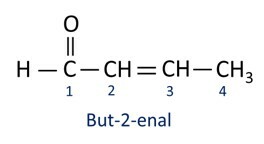
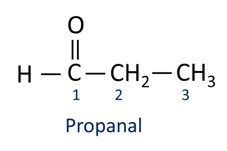
Aldehidi se industrijsko uporabljajo pri izdelavi parfumov in aroma, saj se njen vonj in okus razlikujeta glede na dolžino ogljikove verige. Aldehidne spojine se med drugim uporabljajo tudi pri izdelavi čistil, zdravil, polimerov itd. Aldehidi s kratko ogljikovo verigo se lahko uporabljajo kot sredstvo za ohranitev, kot je slavni formalin, ki je aldehid z imenom metanal.

karboksilna kislina
Funkcijo organske karboksilne kisline prepoznamo po prisotnosti karboksilne funkcionalne skupine (-COOH).
Funkcionalna skupina karboksilnih kislin: –(C=O)OH ali –COOH.

Spojine s to organsko funkcijo so šibke kisline, saj zlahka sproščajo H ione+ v vodni raztopini.
A nomenklatura za karboksilne kisline sledi pravilom Iupac, vendar se izraz "kislina" pojavi pred predpono, ki označuje število ogljikovih ogljikov, uporabljena pripona pa je -oic.
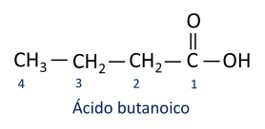
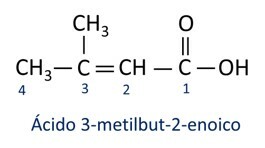
O Najpogostejša karboksilna kislina v vsakdanjem življenju je Ocetna kislina, snov, ki je prisotna v kisu. Vitamin C, ki ga je veliko v številnih citrusih, je organska molekula, imenovana askorbinska kislina.
Ester
Funkcija organskega estra prepoznamo po prisotnosti karbonilne funkcionalne skupine, katerega ogljikov atom ima kisikov ligand.
Funkcionalna skupina estrov: –R–(C=O)O–R'.
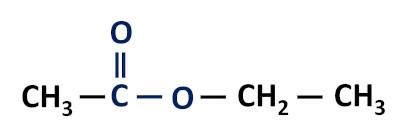
Estri so derivati karboksilnih kislin, ki se od teh razlikujejo po tem, da imajo alkilni radikal vezan na atom kisika namesto na atom vodika.
Molekule, ki pripadajo estrski funkciji, nastanejo z reakcijo med karboksilno kislino in alkoholom, reakcijo, znano kot esterifikacija.
Pravila za nomenklatura estrov definiral Iupac, menijo, da je molekula sestavljena iz dveh delov:
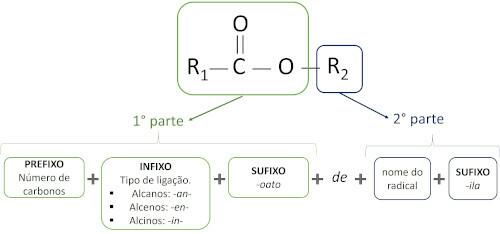
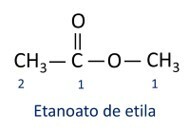
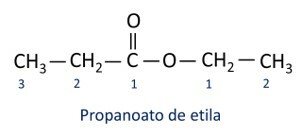
Glavna značilnost estrov je njihova sposobnost simulacije okusa in arome naravnih živil, glede na dolžino ogljikovih verig (R1 in R2). Zaradi tega se estri pogosto uporabljajo kot arome v živilski industriji, v proizvodnji farmacevtskih izdelkov, parfumov in kozmetike.
Eter
Organska funkcija etra je označen s tem, da ima atom kisika med dvema ogljikovima verigama.
Funkcionalna skupina etrov: R–O–R.

Etri so lahko vnetljive snovi z značilnim in močnim vonjem.
A uradna nomenklatura Iupac za etre sledi vrstnemu redu predpona + pripona + pripona. Vendar stran molekule, ki ima manj ogljikovih atomov, dobi pripono -oksi, medtem ko se daljša veriga ogljika poimenuje, kot da bi bila ogljikovodik, in dobi pripono -o.
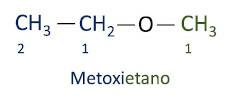
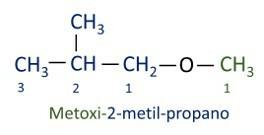
Etri so uporabljajo se kot topila za barve, smole, olja in maščobe. Posledično se uporabljajo v različnih industrijskih in farmacevtskih procesih. Eter so nekoč uporabljali kot anestetik, danes pa so ga nadomestile druge varnejše snovi.
Preberite tudi:Nitro spojine — spojine, ki vsebujejo nitro (NO2) skupine v svoji molekuli
Rešene vaje o funkcijah kisika
Vprašanje 1
(Uece) V organski kemiji je funkcionalna skupina opredeljena kot molekularna struktura, ki daje snovem podobno kemično obnašanje. Niz spojin, ki imajo isto funkcionalno skupino, imenujemo organska funkcija. Označi možnost, ki pravilno predstavi spojino in organsko funkcijo, ki ji pripada.

Resolucija:
Črka C
Med alternativami je edina, ki pravilno izraža funkcionalno skupino k imenu kemijske funkcije, točka C. Funkcijo organskega estra definira karbonilna funkcionalna skupina, katere ogljikov atom ima tudi kisikov ligand.
V točki A je izražena etrska funkcionalna skupina.
V točki B je izražena ketonska funkcionalna skupina.
V točki D je izražena amidna funkcionalna skupina. amini je amidi spadajo med dušikove funkcije.
vprašanje 2
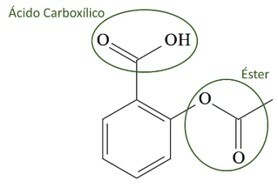
(UCS-RS) V 5. stoletju pr. C., Hipokrat, grški zdravnik, je zapisal, da izdelek iz vrbovega lubja lajša bolečine in znižuje vročino. Ta isti izdelek, kisli prah, je omenjen celo v besedilih starodavnih civilizacij Bližnjega vzhoda, Sumerja, Egipta in Asirije. Ameriški staroselci so ga uporabljali tudi proti glavobolom, vročini, revmi in tresavicam. To zdravilo je predhodnik aspirina, katerega kemična struktura je prikazana spodaj.
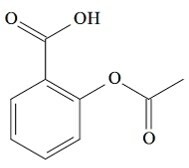
Organske funkcije, prisotne v strukturi aspirina, predstavljene zgoraj, so:
a) karboksilna kislina in ester.
b) alkohol in eter.
c) amin in amid.
d) amin in eter.
e) aminokislina in alkohol.
Resolucija:
črka a
Avtor: Ana Luiza Lorenzen Lima
Učiteljica kemije
Vir: Brazilska šola - https://brasilescola.uol.com.br/quimica/funcoes-oxigenadas.htm


