THE Zakon o hitrosti reakcije povezuje hitrost kemične preobrazbe s koncentracijami reagentov v količini snovi (mol / l), ki jo lahko navedemo na naslednji način:

Na primer, upoštevajte naslednjo generično reakcijo:
aA + bB → cC + dD
Recimo, da povečamo koncentracijo reaktantov A in B, kaj se bo zgodilo s hitrostjo reakcije? No, ker se bo v istem prostoru povečala količina reaktantnih delcev, bo med njimi prišlo do učinkovitejših trkov, kar bo povzročilo povečanje hitrosti razvoja reakcije. Kar pomeni, da bo povečala vašo hitrost.
Zato je hitrost reakcije neposredno sorazmerna s koncentracijo reaktantov. Je pa odvisno tudi od temperature. Zato imamo naslednjo matematično enačbo, ki predstavlja zakon reakcijske hitrosti:

Na čem:
v = hitrost reakcije;
k = konstanta, ki je odvisna samo od vrednosti temperature;
α in β = eksperimentalno določeni eksponenti.
Šele ko je reakcija osnovna, torej v enem koraku, so eksponenti popolnoma enaki koeficientom uravnotežene kemijske enačbe: v = k. [THE]The. [B]B
. V drugih primerih pa je treba poskusno določiti primerno jakost, do katere je treba povišati koncentracijo vsakega reagenta.Zakon hitrosti reakcij se imenuje več, tukaj je nekaj: Zakon o množičnem delovanju, enačba hitrosti, kinetični zakon reakcije in zakon Guldberg-Waage.
Poglejmo primer uporabe tega zakona:
Upoštevajte naslednjo osnovno reakcijo:
2 HCl (g) → H2 (g) + Kl2 (g)
a) Napišite enačbo za hitrost te reakcije;
b) S poskusi smo v spodnji tabeli zabeležili hitrost reakcije razgradnje vodikovega klorida in koncentracijo tega reagenta pri konstantni temperaturi 25 ° C:
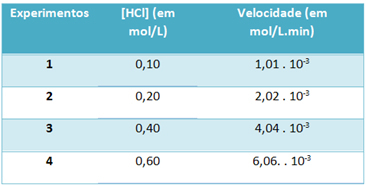
Na podlagi tega določimo značilno konstanto hitrosti te reakcije pri omenjeni temperaturi.
Resolucija:
The) v = k. [HCl]2
b) v = k. [HCl]2
k = __v___
[HCl]2
k = 1,01. 10-3 mol. L-1. min-1
0,01 mol. L-1
k = 1,01. 10-1 min-1
Za rešitev črke “b” lahko uporabite podatke katerega koli od poskusov, da bo dobljena vrednost enaka.
Kaj pa, če reakcija ni osnovna? Kako bo mogoče takšna vprašanja razrešiti v neelementarnih reakcijah? Če želite izvedeti, kako, preberite zakon hitrosti za neelementarne reakcije.
Avtorica Jennifer Fogaça
Diplomiral iz kemije
Vir: Brazilska šola - https://brasilescola.uol.com.br/quimica/lei-velocidade-das-reacoes-quimicas.htm
