THE destilacija je metoda ločevanja homogenih zmesi, to je, ko so komponente v eni sami fazi.
Obstajata dve vrsti destilacije. Preprosta destilacija se uporablja pri ločevanju trdnih snovi in tekočin in frakcijski destilaciji v mešanici tekočin, ki se med seboj mešajo.
Da bi lahko izolirali določeno komponento zmesi, je treba spremeniti spremenljivko. V primeru destilacije pride do ločevanja s spremembo temperature, tako da komponenta, ki nas zanima, spremeni svoje agregatno stanje.
Lastnost snovi, ki se uporabljajo v tem procesu, je vrelišče, to je temperatura, pri kateri pride do prehoda iz tekočine v plin.
proces destilacije
Postopek destilacije je sestavljen iz dovajanja toplote zmesi, dokler se ne doseže vrelišče komponente, ki nas zanima, in ta preide v plinasto stanje, pri čemer se loči od drugih.
Po tem plin prehaja skozi hladilni stolpec, kjer se toplota odvaja od snovi, dokler ne doseže tališča in se tako vrne v tekoče stanje. Ta material se usmeri v drugo posodo.
preprosta destilacija
Za ločevanje homogene zmesi trdna snov, raztopljena v tekočini uporablja se preprosta destilacija.
Na spodnji sliki lahko vidimo osnovno opremo za postopek ločevanja.

Ali so:
- Destilacijsko bučko (1), ki vsebuje zmes;
- Grelna odeja (2), ki mešanici zagotavlja toploto;
- Termometer (3) za spremljanje spremembe temperature;
- Kondenzator (4), za hlajenje izhlapene komponente in
- Čaša (5) za zbiranje ločene komponente v tekočem stanju.
Ta postopek se lahko uporablja na primer za ločevanje natrijevega klorida (NaCl), znanega kot namizna sol, in vode. Sol ima vrelišče 1465 °C in se raztopi v vodi, da nastane homogena zmes.
Ker ima voda vrelišče 100 ºC, se zlahka spremeni v plinasto stanje in se loči od zmesi, sol pa kristalizira in ostane v trdnem stanju v posodi.
Vodna para izstopa na vrhu destilacijske bučke in prehaja skozi kondenzator. Po stenah te opreme kroži hladna ali hladna voda. Izmenjava toplote med tekočinami povzroči, da ločena komponenta zmesi izgubi toploto in se vrne v tekoče stanje, da se zbere v drugi posodi. Ta tekočina se imenuje destilat.
frakcijska destilacija
Za ločevanje homogene zmesi tekočine, ki se med seboj mešajo in z veliko razliko med temperaturami vrelišča se uporablja frakcijska destilacija.
Ta metoda je frakcionirana, ker so komponente ločene od mešanice naraščajočem vrstnem redu vrelišča, torej začenši z najnižjo do tiste, ki zahteva najvišjo temperaturo za spremembo faze.
Na spodnji sliki je oprema, ki se uporablja za izvedbo metode.
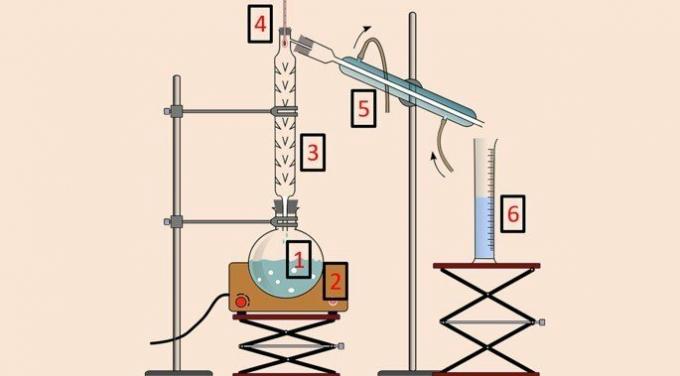
Kot pri preprosti destilaciji se uporablja destilacijsko bučko (1), grelno odejo (2), termometer (4), kondenzator (5) in čašo (6). Vendar pa je destilacijsko ali frakcionacijsko kolono (3) je oprema, ki omogoča ločevanje glede na temperaturo.
Destilacijski stolpec ima v sebi vrsto ovir, ki preprečujejo, da bi se vse sestavine mešanice hkrati izhlapevale.
Ta postopek se pogosto uporablja za ločevanje frakcij nafte, ki je mešanica ogljikovodikov. Nekatere sestavine nafte in njihova vrelišče (PE) so: butan (PE 20 ºC), bencin (PE 150 ºC) in kerozin (PE 300 ºC).
S frakcijsko destilacijo se najprej loči butan, saj ima najnižje vrelišče, nato bencin z vmesnim vreliščem in na koncu petrolej.
Aplikacije za destilacijo
Destilacija se pogosto uporablja v industriji, saj je veliko mešanic podvrženo temu procesu. Po tej metodi se izdelujejo žgane pijače, kot so viski, žganje in vodka.
Petrokemična industrija uporablja frakcijsko destilacijo za rafiniranje nafte. Destilacijski stolpi so velike strukture, izdelane za ločevanje frakcij tega fosilnega goriva.

Destilacijske vaje
Vprašanje 1
Destilacija je metoda ločevanja, ki temelji na lastnostih.
kemijo
b) Fizika
c) Biološki
d) Splošno o zadevi
Alternativa: b) Fizika.
Vrelišče je specifična fizikalna lastnost snovi, saj je lastna določeni snovi. To je temperatura, pri kateri material preide iz tekočega v plinasto stanje, to pomeni, da je podvržen izhlapevanju.
vprašanje 2
To so primeri mešanic, ločenih z destilacijo, RAZEN
a) voda + aceton
b) slanica
c) voda + olje
d) morska voda
Pravilna alternativa: c) voda + olje.
Voda in olje sta nemešljivi snovi. V tem primeru se za ločevanje sestavin mešanice uporablja metoda dekantiranja. Ta metoda temelji na razliki v gostoti.
Slanico (voda + sol) in morsko vodo, ki ima tudi raztopljene soli, ločimo s preprosto destilacijo. Za vodo in aceton se uporablja frakcijska destilacija.
vprašanje 3
(UFRGS) Dvofazni heterogeni sistem tvorijo tri različne tekočine A, B in C. Znano je, da:
A in B se med seboj mešata;
C se ne meša z A in B;
A je bolj nestanoviten kot B.
Na podlagi teh informacij so najprimernejše metode za ločevanje treh tekočin:
a) centrifugiranje in dekantiranje.
b) dekantiranje in frakcijsko taljenje.
c) filtriranje in centrifugiranje.
d) filtracijo in frakcijsko destilacijo.
e) dekantacija in frakcijska destilacija.
Pravilna alternativa: e) dekantacija in frakcijska destilacija.
Heterogen sistem vprašanja ima dve fazi:
1. faza: tekočini A in B, ki se med seboj mešata
Faza 2: tekočina C, ki se ne meša z drugimi komponentami
Zato se faza 1 zaradi razlike v gostoti loči od faze 2 z metodo dekantiranja. Zaradi razlike v temperaturi vrelišča, ker je A bolj hlapen kot B, to pomeni, da zlahka preide v plinasto stanje, se uporablja frakcijska destilacija.
Pridobite več znanja z vsebinami:
- Enostavna in frakcijska destilacija
- Ločevanje mešanic
- Vaje za ločevanje mešanic