Višja kot je temperatura, večja je hitrost reakcije.
To lahko zlahka opazimo v mnogih situacijah našega vsakdana, kot v naslednjih primerih:
- Ko želimo upočasniti reakcijo razgradnje živila, znižamo temperaturo in jo postavimo v hladilnik;

- Če želimo pospešiti reakcijo kuhanja hrane, jo preprosto položimo v kuhalnik. tlak, ki z naraščajočim tlakom povečuje tudi temperaturo vrelišča tekoče vode, v kateri je hrana je;

- Požari so na splošno uničujoči, ker se temperatura okolja poveča, kar povzroči povečanje hitrosti reakcije izgorevanja;
- Za upočasnitev metaboličnih kemijskih procesov, kar zmanjšuje možnosti za poškodbe možganov zaradi pomanjkanje kisika, nekatere operacije izvajamo tako, da znižamo bolnikovo telesno temperaturo in dosežemo okoli 15 ° C;
- Če damo šumečo tableto v kozarec vroče vode in drugo v kozarec hladne vode, se bo prva veliko hitreje raztopila.
Kaj pa pojasnjuje neposredno sorazmeren vpliv temperature na hitrost reakcije?
Kot je razloženo v besedilu „Pogoji za pojav kemičnih reakcij
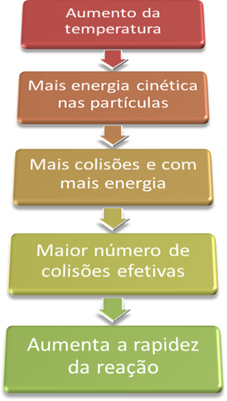
", Da reakcija teče, je treba izpolniti nekatere pogoje, na primer delce trčiti morajo učinkovito in z minimalno potrebno energijo, ki se imenuje aktivacijska energija.Tako ko povečamo temperaturo sistema, povečamo tudi vznemirjenost reagirajočih delcev in jim zagotovimo več kinetične energije. S tem se bo zgodilo več trkov in z več energije bo povečala količino delcev, ki bodo reagirali in posledično povečala hitrost reakcije.
Avtorica Jennifer Fogaça
Diplomiral iz kemije
Vir: Brazilska šola - https://brasilescola.uol.com.br/quimica/temperatura-velocidade-das-reacoes.htm


