Oksidacija je ime za proces izgube elektronov zaradi atoma, skupine ali ionske vrste med a kemijska reakcija. Prepoznava se po povečanju NOX (oksidacijsko število) vrste ali atoma pri primerjavi reaktanta in produkta.
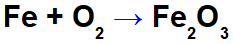
Enačba oksidacije železa.
V zgornji enačbi lahko na primer navedemo NOX vsakega od udeležencev:
Reagentno železo (Fe): ima NOX 0, saj je a preprosta snov;
Kisik v reagentu (O): ima NOX 0, ker je preprosta snov;
Kisik v izdelku: vsebuje NOX -2, ker ni povezan z alkalijsko kovino, alkalna zemlja ali nastajanje vodika peroksidi oz superoksidi;
Železo v izdelku: vsebuje NOX +3, ker mora vsota NOX železa, pomnožena z 2 (število atomov) + NOX kisika, pomnožena s 3, dati 0, saj je sestavljena snov:
x, 2 + 3.(-2) = 0
2x - 6 = 0
2x = +6
x = + 6
2
x = +3
Če primerjamo NOX reagentnega železa (0) s produktom (+3), smo opazili povečanje, to je, da je bil podvržen procesu oksidacija. Omeniti velja, da je pojav oksidacija vedno ga spremlja pojav redukcije (kar pomeni pridobitev elektronov), ki ga prepoznamo z zmanjšanjem NOx, kot se v primeru zgodi s kisikom.
Ne nehaj zdaj... Po reklami je še več ;)
Preberite tudi:Določanje oksidacijskega števila (NOX)
Primeri situacij, v katerih pride do oksidacije:
1. Zgorevanje

Zgorevanje materiala kaže tudi na oksidacijo.
Zgorevanje je vsaka kemična reakcija, ki se pojavi v prisotnosti a gorivo kateri koli in oksidirajoči plin kisik (O2), kar ima za posledico proizvodnjo toplote in svetlobe. Pri vsakem zgorevanju se pojavi reakcija oksidacija.
2. Nekatere organske reakcije
V vsaki organski reakciji, ki poteka v prisotnosti spodaj navedenih sredstev, je proces oksidacija:
Kalijev dikromat (K2Kr2O7) ali kalijevega permanganata (KMnO4);
Prisotnost močne kisline ali močne baze;
Plin ozon (O3) v prisotnosti kovinskega cinka (Zn) in vode (H2O).
3. Baterije ali baterije

Baterije so naprave, pri katerih vedno pride do oksidacije.
Skladi ali baterije so elektrokemične naprave, ki hranijo kemične snovi. Ena od teh snovi bo podvržena oksidaciji, druga pa redukciji, kar povzroči nastanek električnega toka.
4. Elektroliza
Elektroliza je kemični proces, pri katerem je vodna raztopina, ki vsebuje sol, izpostavljena električnemu toku, ki na koncu spodbuja oksidacijo anionov, prisotnih v teh materialih. Pri vseh elektrolizah obstaja oksidacija.
Jaz, Diogo Lopes Dias
Ali se želite sklicevati na to besedilo v šolskem ali akademskem delu? Poglej:
DNI, Diogo Lopes. "Kaj je oksidacija?"; Brazilska šola. Na voljo v: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-oxidacao.htm. Dostop 27. julija 2021.
