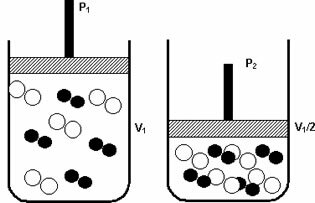
Vrenje je prehod iz tekočega v plinasto stanje. To se zgodi, ko del tekočine pod pritiskom prejme toploto in doseže določeno temperaturo.
Količina toplote, ki jo mora telo prejeti, da se popolnoma spremeni v hlape, je odvisna od snovi, ki jo sestavlja.
Snov v tekočem stanju nima določene oblike, ob predpostavki oblike posode, ki jo vsebuje.
Ker je praktično nerazumljiv, predstavlja kohezijsko silo med delci, ki ga sestavljajo.
Za prehod v plinasto stanje mora snov prejemati toploto. Zaradi tega povečanja energije bodo molekule vibrirale z večjo intenzivnostjo, kar bo povečalo razdaljo med njimi.
Na ta način kohezijska sila praktično ne obstaja. Telo v tem stanju nima določene oblike ali volumna.
Gejzirji so primeri vrenja, ki se zgodi s podtalnico v vulkanskih regijah. Magma segreje vodo in ko doseže določeno temperaturo, začne spreminjati stanje.
Para zavzema večjo prostornino in povečuje tlak v podzemni votlini. Posledično se mešanica hlapov in tekočine skozi majhne razpoke izloči na površino.

Značilnosti vrenja
Tekočina vre po naslednjem vzorcu:
- Ob ohranjanju konstantnega tlaka bo temperatura skozi ves čas vrenja ostala konstantna.
- Količina toplote na masno enoto, ki je potrebna, da se tekočina popolnoma spremeni v paro, se imenuje latentna toplota uparjanja. Njegova vrednost je odvisna od snovi, ki sestavlja tekočino.
- Temperatura, pri kateri vsaka snov vre, je dobro določena in se imenuje vrelišče.
Namig: Ko kuhamo hrano, je dobro, da ogenj prižgemo, ko voda zavre. Ker temperatura ves čas vrenja ostaja enaka, bo čas kuhanja enak pri visoki vročini ali nizki vročini. Na ta način prihranimo plin in okolje je hvaležno.
Količina latentne toplote
Količina toplote, ki jo mora tekočina sprejeti, da se spremeni v paro, je odvisna od vrednosti latentne toplote uparjanja in njene mase.
Spodaj predstavljamo vrednost latentne toplote uparjanja nekaterih snovi:

Formula
Za izračun količine toplote, ki je potrebna za spremembo stanja tekočine, uporabimo naslednjo formulo:
Kje,
Vv: količina toplote (apno)
m: masa (g)
Lv: latentna toplota uparjanja (kal / g)
Primer:
Koliko toplote je potrebno, da 100 g etanola zavre in se popolnoma spremeni v paro?
Vv = 100. 204 = 204 000 kal
Temperatura vrelišča
Temperatura, pri kateri telo vre, je odvisna od snovi, ki jo sestavlja, in tlaka, ki mu je podvrženo.
Vrelišče snovi se določi v laboratoriju. Na primer, vrelišče vode v 1 atmosferi je 100 ° C. Železo je 2800 ° C, medtem ko je vodik - 252,8 ° C.
Če želite vedeti tudi temperaturo fazne spremembe drugih snovi, preberite tudi vrelišče.
Manjši kot je pritisk telesa, nižje je njegovo vrelišče. To pomeni, da v mestih z veliko nadmorsko višino kuhanje hrane traja veliko dlje.
Za hitrejše kuhanje hrane uporabljamo lonce pod pritiskom. Ta vrsta štedilnika uporablja tesnilni sistem, zaradi katerega je tlak v njem večji od atmosferskega.
Višji tlak poveča tudi vrelišče. V primeru vode bo vrela pri temperaturi, ki lahko doseže 120 ºC, kar skrajša čas kuhanja.
fazne spremembe
Splošno se imenuje prehod iz tekočega v plinasto stanje izhlapevanje, ki poleg vrenja zajema še dva postopka: izhlapevanje in ogrevanje.
Izhlapevanje poteka postopoma, pri čemer ni treba doseči določene temperature. Po drugi strani pa pride do segrevanja, ko tekočino postavimo na površino, ki ima temperaturo nad vreliščem.
Obstajajo še drugi procesi spremembe stanja. Ali so:
- Fuzija
- Utrjevanje
- Utekočinjenje ali kondenzacija
- Sublimacija
V spodnjem diagramu predstavljamo tri fizikalna stanja snovi in ustrezne spremembe stanja:
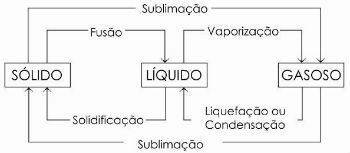
Če želite izvedeti več, preberite tudi vi Fizična stanja vode.
Vaje
Enem - 1999
Besedilo je treba uporabiti za naslednji dve vprašanji.
Tlačni štedilnik omogoča kuhanje hrane v vodi veliko hitreje kot običajni štedilniki. Njegov pokrov ima gumijasto tesnilo, ki ne pušča pare, razen skozi osrednjo luknjo, na kateri stoji utež, ki nadzoruje tlak. Med uporabo se v notranjosti kopiči visok tlak. Za njegovo varno delovanje je treba paziti na čistočo osrednje luknje in obstoj varnostnega ventila, ki se običajno nahaja v pokrovu.
Shema tlačnega štedilnika in diagram vodne faze sta predstavljena spodaj.
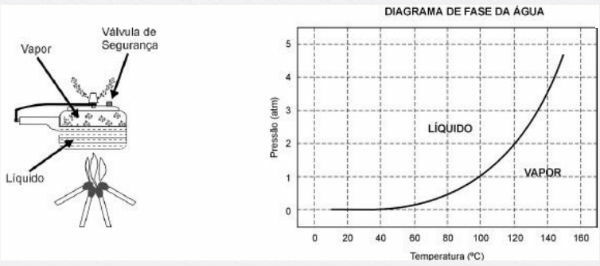
1) Prednost uporabe lonca pod pritiskom je hitrost kuhanja hrane, kar je posledica
a) tlak v njem, ki je enak tlaku zunaj.
b) temperatura njegove notranjosti, ki je nad temperaturo vrelišča vode v kraju.
c) količina dodatne toplote, ki se prenese v posodo.
d) količina pare, ki jo sprošča ventil.
e) debelina stene, ki je večja od debeline običajnih ponv.
Alternativa b: pri notranji temperaturi, ki je nad temperaturo vrelišča vode v prostoru.
2) Če zaradi varčevanja znižamo toploto pod loncem pod pritiskom takoj, ko para izstopi skozi ventil, da preprosto ohranimo čas vrenja, čas kuhanja
a) večja bo, ker se ponev "ohladi".
b) bo manjša, saj zmanjšuje izgubo vode.
c) bo večja, ko se tlak zmanjša.
d) bo večja, ko se izhlapevanje zmanjša.
e) se ne bo spreminjala, saj se temperatura ne spreminja.
Alternativa e: ne bo spremenjena, ker se temperatura ne spreminja.