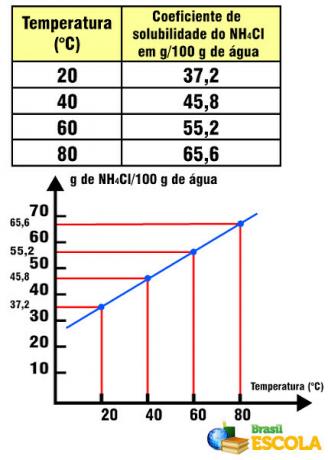
Elektroliza je a nespontana kemijska reakcija ki vključuje oksidacijsko-redukcijsko reakcijo, ki jo povzroči električni tok.
Za elektrolizo mora biti vključeni električni tok neprekinjen in imeti zadostno napetost.
Da imajo vključeni ioni svobodo pri gibanju, ki ga izvajajo, lahko pride do elektrolize s fuzijo (magmatska elektroliza) ali z raztapljanjem (elektroliza v raztopini).
Uporaba elektrolize
Iz postopka elektrolize nastane veliko materialov in kemičnih spojin, na primer:
- aluminij in baker
- vodik in klor v valju
- bižuterija (postopek galvanizacije)
- lonec na pritisk
- magnezijevo kolo (avtomobilske pokrovčke).
Zakoni elektrolize
Zakone elektrolize je razvil angleški fizik in kemik Michael de Faraday (1791-1867). Oba zakona urejata kvantitativne vidike elektrolize.
THE prvi zakon elektrolize ima naslednjo izjavo:
“Masa elementa, naloženega med postopkom elektrolize, je neposredno sorazmerna s količino električne energije, ki prehaja skozi elektrolitsko celico”.
Q = i. t
Kje,
V: električni naboj (C)
jaz: jakost električnega toka (A)
t: časovni interval prehoda električnega (-ih) toka (-ov)
THE drugi zakon elektrolize ima naslednjo izjavo:
“Mase različnih elementov, ki se med elektrolizo nalagajo z enako količino električne energije, so sorazmerne njihovim kemijskim ekvivalentom”.
M = K. IN
Kje,
M: masa snovi
K: konstanta sorazmernosti
IN: gramov ekvivalent snovi
Več o tem v članku: Faradayeva stalnica.
Razvrstitev
Postopek elektrolize lahko poteka s taljenjem ali raztapljanjem:
Magmatska elektroliza
Magmatska elektroliza je tista, ki se predela iz staljenega elektrolita, to je s postopkom Fuzija.
Kot primer uporabimo NaCl (natrijev klorid). Ko snov segrejemo na 808 ° C, se ta stopi in prisotni ioni (Na+ in Cl-) imajo zdaj večjo svobodo gibanja v tekočem stanju.
ko električni tok prehaja v elektrolitsko celico, katione Na+ privlači jih negativni pol, imenovan katoda. Že anioni Cl-, privlačijo pozitivni pol ali anoda.
V primeru Na+ pride do reakcije redukcije, medtem ko pri Cl-, je reakcija oksidacija.
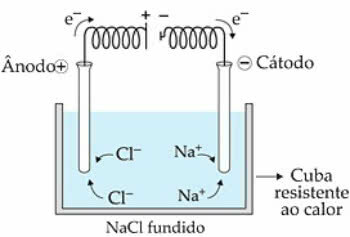
Shema magmatske elektrolize NaCl
Vodna elektroliza
Pri vodni elektrolizi je uporabljeno ionizirajoče topilo voda. V vodni raztopini lahko elektrolizo izvedemo z obrnjenimi ali aktivnimi (ali reaktivnimi) elektrodami.
Inertne elektrode: voda v raztopini ionizira po enačbi:
H2O ↔ H+ + OH-
Z disocijacija NaCl imamo:
NaCl → Na+ + Kl-
Tako kationi H+ in naprej+ se lahko izpraznijo na negativnem polu, medtem ko OH anioni- in Cl- se lahko izprazni na pozitivnem polu.
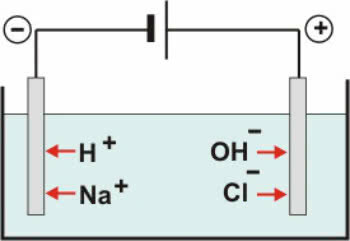
Shema vodne elektrolize NaCl
Pri kationih pride do reakcije redukcije (katodna redukcija), pri anionih pa do reakcije oksidacije (anodna oksidacija).
Tako imamo reakcijo elektrolize:
2 NaCl + 2H2O → 2 In+ + 2 OH- + H2 + Kl2
Iz tega lahko sklepamo, da molekule NaOH ostanejo v raztopini, medtem ko H2 se sprosti na negativnem polu in Cl2, na pozitivnem polu.
Rezultat tega postopka bo enakovredna enačba:
2 NaCl + 2H2O → 2 NaOH + H2 + Kl2
Aktivne elektrode: v tem primeru aktivne elektrode sodelujejo pri elektrolizi, vendar trpijo zaradi korozije.
Kot primer imamo elektrolizo v vodni raztopini bakrovega sulfata (CuSO4):
CUSO4 → Cu2 + OS 2-4
H2O → H+ + OH-
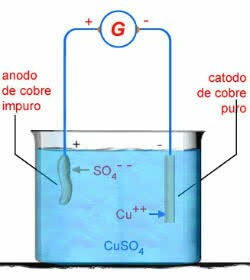 Shema vodne elektrolize CuSO4
Shema vodne elektrolize CuSO4
V tem primeru bo bakrena anoda korodirala:
Ass0 → Cu2+ + 2e-
To je zato, ker v skladu s standardnimi potenciali elektrod električni tok lažje odstrani elektrone iz Cu0 kot OS 2-4 ali od oh-.
Zato se na negativnem polu pojavi naslednja reakcija elektrolize:
2e- + Cu2+ → Cu
Na pozitivnem polu imamo reakcijo elektrolize:
Cu → Cu2+ + 2e-
Na koncu, ko dodamo še dve enačbi elektrolize, imamo kot rezultat nič.
Bi radi izvedeli več o temi? Preberite članke:
- Ion, Kation in Anion
- Kemijske reakcije
- Reakcije oksidacije
Baterija in elektroliza
Elektroliza temelji na nasprotnem pojavu v primerjavi z baterijo. Pri elektrolizi postopek ni spontan, kot se dogaja v baterijah. Z drugimi besedami, elektroliza pretvori električno energijo v kemično energijo, medtem ko celica proizvaja električno energijo iz kemične energije.
vedeti več o Elektrokemija.
Vaje
1. (Ulbra-RS) Kovinski kalij lahko dobimo z magmatsko elektrolizo kalijevega klorida. V tej izjavi označite pravilno možnost.
a) Elektroliza je postopek, ki vključuje oksidacijsko-redukcijske in redukcijske reakcije, ki jih spodbuja električni tok.
b) Magmatska elektroliza kalijevega klorida poteka pri sobni temperaturi.
c) Kalij najdemo v naravi v zmanjšani obliki (K0).
d) Elektrolizna reakcija poteka s pomočjo ultravijoličnega sevanja.
e) V procesu elektrolize kalijevega klorida, da dobimo kovinski kalij, pride do prenosa elektronov iz kalija v klor.
Alternativa
2. (UFRGS-RS) V katodi elektrolizne celice je vedno:
a) Nanašanje kovin.
b) Zmanjšanje polovične reakcije.
c) Proizvodnja električnega toka.
d) Sproščanje vodikovega plina.
e) Kemična korozija.
Alternativa b
3. (Unifor-CE) Naslednji predlogi se nanašajo na elektrolizo:
JAZ. Pri porabi električne energije pride do reakcij elektrolize.
II. Vodnih raztopin glukoze ni mogoče elektrolizirati, ker ne prevajajo električnega toka.
III. Pri elektrolizi solnih raztopin se kovinski kationi oksidirajo.
Lahko rečemo, da samo:
a) Prav imam.
b) II je pravilen.
c) III je pravilen.
d) I in II sta pravilna.
e) II in III sta pravilna.
Alternativa
4. (FEI-SP) Dva študenta kemije sta izvedla BaCl elektrolizo2; prvi voden, drugi pa ognjen. Glede rezultata lahko rečemo, da sta oba dobila:
a) H2 to je2 na anodah.
b) H2 in Ba na anodah.
c) Cl2 in Ba na elektrodah.
d) H2 na katodah.
e) Cl2 na anodah.
Alternativa in
5. (Vunesp) "Bazen brez kemije"Je oglas, ki vključuje čiščenje vode. Znano pa je, da je zdravljenje sestavljeno iz dodajanja natrijevega klorida vodi in prenosa tega vode skozi posodo, opremljeno z bakreno in platinsko elektrodo, povezano s svincem avto.
a) Na podlagi teh informacij se pogovorite o pravilnosti oglasnega sporočila
b) Glede na inertne elektrode napiši enačbe vključenih reakcij, ki upravičujejo prejšnji odgovor.
a) Sporočilo v oglasu ni pravilno, saj bodo nastali kemični proizvodi.
b) 2 NaCl + 2H2O → 2 NaOH + H2 + Kl2 (reakcija, ki tvori klor, koristen pri čiščenju vode v bazenu)
2 NaOH + Cl2 → NaCl + NaClO + H2O (reakcija, ki tvori NaClO, močan baktericid)