je poklican večplastna elektronska distribucija porazdelitev, ki upošteva samo količino elektroni največ v vsakem od slojev (glede na Bohrov atom) atoma.
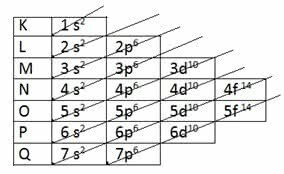
Sloji, ki jih ima lahko atom, so K, L, M, N, O, P in Q. Oglejte si največjo količino elektronov v vsakem od njih:
K = 2 elektrona
L = 8 elektronov
M = 18 elektronov
N = 32 elektronov
O = 32 elektronov
P = 18 elektronov
Q = 8 elektronov
Za izvedbo a elektronska distribucija v plasteh, potrebno je:
Spoznajte atomsko število atoma, ki bo obdelan, saj to število označuje število elektronov;
Spoštujte mejo elektronov vsake lupine, kot je opisano zgoraj.
Previdno upoštevajte vsa spodnja pravila:
→ 1. pravilo: Če je število elektronov zadostno, morata prva (K-lupina) in druga (K-lupina) lupina atoma vedno sprejeti največje število elektronov, ki sta 2 oziroma 8;
→ 2. pravilo: Predzadnja lupina, ki sprejema elektrone, nikoli ne more preseči meje 18 elektronov;
→ 3. pravilo: Zadnja lupina, ki sprejme elektrone, ne more nikoli preseči meje osmih elektronov;
→ Pravilo 4:
Kadar je v zadnji lupini več elektronov, kot jih lahko spravimo, moramo vedno ponoviti število elektronov iz prejšnje lupine, preostale elektrone pa položiti v naslednjo lupino.Oglejte si nekaj primerov večplastna elektronska distribucija:
Primer 1: Večplastna razporeditev elementa natrij, katerega atomsko število je 11.
Ker je atomsko število natrija 11, imajo njegovi atomi 11 elektronov. Njegova distribucija bo izvedena na naslednji način:
Sloj K: 2 elektrona
Od enajstih elektronov bo K lupina sprejela le dva, saj je to njena elektronska meja. (pravilo 1).
Sloj L: 8 elektronov
Od preostalih devetih elektronov bo L lupina sprejela le osem, saj je to njena elektronska meja. (pravilo 2).
Sloj M: 1 elektron
Ker je od enajstih, ki jih je imel atom natrija, ostal le en elektron, ga je treba položiti v lupino M, ki je naslednja po lupini L.
Ne ustavi se zdaj... Po oglaševanju je še več;)
2. primer: Večplastna porazdelitev elementa kalcija, katerega atomsko število je 20.
Ker je atomsko število kalcija 20, imajo njegovi atomi 20 elektronov. Njegova razporeditev po plasteh bo izvedena na naslednji način:
Sloj K: 2 elektrona
Od 20 elektronov bo K lupina sprejela le 2 elektrona, saj je to njena elektronska meja. (pravilo 1).
Sloj L: 8 elektronov
Od preostalih 18 elektronov bo L lupina sprejela le 8, saj je to njena elektronska meja. (pravilo 2).
Sloj M: 8 elektronov
Po polnjenju lupin K in L ostane 10 elektronov. Ker zadnja lupina ne more imeti več kot osem elektronov, moramo ponoviti število elektronov iz prejšnje lupine (L lupina), ostale pa postaviti v naslednjo lupino (N lupina) (pravilo 4).
Sloj N: 2 elektrona
Sprejema preostale elektrone, saj jih ni bilo mogoče postaviti v prejšnjo plast (pravilo 4).
3. primer: Večplastna porazdelitev elementa brom, katerega atomsko število 35.
Ker je atomsko število broma 35, imajo njegovi atomi 35 elektronov. Njegova distribucija bo izvedena na naslednji način:
Sloj K: 2 elektrona
Od 35 elektronov bo K lupina sprejela le 2 elektrona, saj je to njena elektronska meja.
Sloj L: 8 elektronov
Od preostalih 33 elektronov bo L lupina sprejela le 8 elektronov, saj je to njena elektronska meja.
Sloj M: 18 elektronov
Ker je ostalo 25 elektronov, lahko ta lupina sprejme le 18 elektronov, saj ne bo zadnja, saj zadnja lahko sprejme le 8, lahko pa zadnja, ki prejme 18. Tako bo plast M predzadnja plast (pravilo 3).
Sloj N: 7 elektronov
Od 35 elektronov, ki jih je imel atom, jih je ostalo le sedem. Ker zadnja lupina lahko sprejme do osem elektronov, bo to zadnja lupina in bo sprejela sedem elektronov.
Jaz, Diogo Lopes Dias
Bi se radi sklicevali na to besedilo v šolskem ali akademskem delu? Poglej:
DNI, Diogo Lopes. "Elektronska stopenjska distribucija"; Brazilska šola. Na voljo v: https://brasilescola.uol.com.br/quimica/distribuicao-eletronica-camadas.htm. Dostopno 28. junija 2021.
Kemija

Niels Bohr, Bohrov atom, atomska fizika, stabilni atom, atomski model, planetarni sistem, plasti elektrosfere, ravni energije, elektronske lupine, elektronska energija, Rutherfordov atomski model, atom vzbujenega stanja.