Kot je razloženo v besedilu „Kataliza in katalizator”, Katalizatorji so kemične vrste, ki pospešujejo hitrost reakcij. Njegova uporaba je zelo koristna v kemični industriji, kjer skušajo prihraniti čim več časa pri proizvodnji.
Vendar je v nekaterih situacijah bolj zanimivo, da reakcija poteka počasneje; kot na primer, ko želite določiti hitrost zelo hitrih reakcij. Da bi dosegli ta podvig, nadzorovali in preučevali te reakcije, je običajno dodati snov, ki upočasni reakcije, ki se imenujejo zaviralci, strupi ali antikatalizatorji.
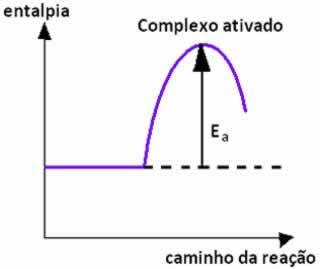
Te kemične vrste se kombinirajo s katalizatorjem, izničijo ali zmanjšajo njegovo delovanje. To je mogoče, ker je mehanizem delovanja katalizatorja zmanjšanje aktivacijske energije, olajšanje reakcijskega procesa in povečanje njegove hitrosti; že inhibitorji delujejo obratno, kar pomeni, da povečajo aktivacijsko energijo, potrebno reaktanti, da dosežejo aktivirani kompleks.
Primer, ki ga lahko omenimo, je arzen (As), ki ima to funkcijo v reakciji Haber-Bosch, reakciji, ki se v industriji pogosto uporablja za proizvodnjo amoniaka z uporabo železa (Fe
(s)) kot njegov katalizator. Tako izkoristek železa postane zelo majhen v prisotnosti arzena, ki ga zavira, to je katalizatorski strup te reakcije, ki je prikazan spodaj: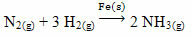
Arzen lahko tudi antikatalitično deluje pri uporabi kovinske platine (Pt(s)) kot katalizator za reakcijo izgorevanja SO2 (g)za proizvodnjo žveplovega trioksida (SO3 (g)). Prisotnost arzena tudi v majhnih količinah izniči katalitično delovanje platine, ki lahko ohromi del proizvodnje. Zato se običajno v panogah, ki se ukvarjajo s to proizvodnjo, uporablja divanijev pentoksid (V2O5 (s)) kot katalizator namesto platine.
Ne ustavi se zdaj... Po oglaševanju je še več;)
Drug primer se pojavi v naslednji reakciji razgradnje vodikovega peroksida:
2 uri2O2 (aq) → 2 H2O(1) + 1 O2 (g)
V tem primeru je zaviralec, ki ga lahko uporabimo, nekaj kisline, ker ko je medij kisel, reakcija poteka počasneje.
Toda inhibitor se v industriji pogosto uporablja tudi predvsem za zaviranje reakcije naravne razgradnje živil, pijač, kozmetike in zdravil.
Kozmetika lahko na primer dolgo traja, da pride do potrošnika; tako se v njih uporabljajo različni konzervansi, na primer propilparaben, ki se uporablja v oljni fazi in deluje protiglivično, in metilparaben, ki se uporablja v vodni fazi in deluje antiseptično. Njihove ustrezne strukture so prikazane spodaj:
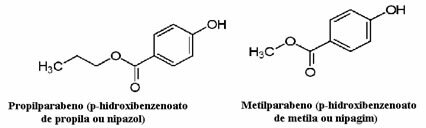
Zanimivo je, da je na številnih kozmetičnih etiketah naslednji stavek: "Ne vsebuje parabenov". To pomeni, da ta kozmetika nima konzervansov, ki smo jih omenili, in da običajno niso testirana na živalih.
Avtorica Jennifer Fogaça
Diplomiral iz kemije
Bi se radi sklicevali na to besedilo v šolskem ali akademskem delu? Poglej:
FOGAÇA, Jennifer Rocha Vargas. "Zaviralci katalizatorja"; Brazilska šola. Na voljo v: https://brasilescola.uol.com.br/quimica/inibidores-catalisador.htm. Dostop 27. junija 2021.