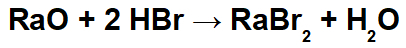Kovine so elementi, za katere je značilna svetlost, trdnost, toplotna in električna prevodnost. So praktično v vseh industrijskih procesih, je prisoten v kovinskih zlitinah, ki se uporabljajo pri izdelavi orodij, nakita in kovancev ter v kemijskih postopkih, kot je redoks, odgovoren za delovanje skladov in baterije.
V periodnem sistemu so razvrščeni na:
polmetal
prehodne kovine
alkalne kovine
zemeljskoalkalijske kovine
V jeklarski industriji so ločeni na:
železne kovine
neželezne kovine
težke kovine
Preberite tudi: Kateri so novi elementi periodnega sistema?
Značilnosti kovin

So večinoma odlični prevodniki toplote in električne energije.
Imajo sijajni videz.
imajo visoko gostoto.
So elektropozitivni elementi (ponavadi tvorijo kation - pozitivne naboje).
Z izjemo Živo srebro, so elementi z visokim tališčem in trdni pri sobni temperaturi.
Imajo mehansko trdnost (trdnost).
So voljni (lahko se oblikujejo, ne da bi se zlomili).
Ne ustavi se zdaj... Po oglaševanju je še več;)
Kovine periodnega sistema
alkalne kovine
Ali so elementi prvi stolpec periodnega sistema, družina 1A. Imenujemo jih alkalijske kovine, ker v mešanju z vodo tvorijo hidrokside, to je alkalno (bazično) raztopino.
Ti elementi v to skupino spadajo:
Litij (li)
Natrij (Ob)
Kalij (K)
Rubidij (Rb)
Cezij (Cs)
Francij (Fr)
Elektronska konfiguracija alkalnih kovin v nevtralnem (nenapolnjenem / ioniziranem) stanju je samo predstavljena elektron v zadnji lupini (valentna plast). O atomski žarek reaktivnost teh kovin pa narašča od zgoraj navzdol (pri opazovanju Periodična tabela). Imajo nizko tališče v primerjavi z drugimi kovinami, so voljni in ne zelo gosti, imajo matiran videz zaradi visok oksidacijski potencial.
Glej tudi:Kakšne so lastnosti snovi?
zemeljskoalkalijske kovine
To so elementi, ki se pojavijo v drugi stolpec periodnega sistema, družina 2A. se imenujejo alkalna zemlja po težnji k tvorjenju raztopin osnovnega (alkalnega) značaja in po zemlji, ker so bili pred 19. stoletjem oksidi, ki jih tvorijo te snovi, označeni tako. Ta izraz je bil uporabljen za označevanje netopnih kovin, ki pri segrevanju niso bile mutirane, skupne značilnosti elementov skupine 2. Kasneje je bilo v luči novih raziskav in poskusov odkrito, da so "zemeljski" elementi dejansko oksidi, ki jih tvorijo kovine.
So kovljive kovine z nizko gostoto dva elektrona v svoji najbolj zunanji lupiniv normalnih pogojih temperature in tlaka so v trdnem stanju. Spadam v to skupino:
Berilij (Bodi)
Magnezij (Mg)
Kalcij (Tukaj)
Stroncij (g.)
Barij (Ba)
Radio (Žaba)
prehodne kovine
sestavljajo skupina B Periodnega sistemain se nahajajo med zemeljskoalkalijskimi kovinami in ametali. IUPAC jih je opredelil kot elemente, ki imajo nepopolno energijsko podplast energéticad. Izraz "prehodne kovine" se nanaša na prehod iz 2. v 13. skupino v periodnem sistemu in naraščajoče dodajanje elektronov v orbiti "d".
Skupino prehodnih kovin sestavljajo gosti elementi z visokim tališčem in vreliščem in manj reaktivni kot kovine skupine 1 in 2 (Družina 1A in 2A). Med prehodnimi kovinami sta volfram, ki je element z najvišjim tališčem (3422 ° C), in živo srebro (Hg), ki je kovina, ki je v normalnih pogojih temperature in tlaka tekoča, ima tališče (-38,83 ° C).
Prehodne kovine imajo različna oksidacijska stanja (NOX spremenljivka) in tvorijo obarvane snovi.

Notranji prehodni elementi
Notranji prehodni elementi so:
Lantanidi: serije, sestavljene iz elementov, ki imajo od 57 do 71 protonov in so, z izjemo prometa, naravni.
Aktinidi: skupina, ki jo tvorijo elementi z atomskim številom od 89 do 103 in ki so večinoma sintetični. Vsa ta skupina je radioaktivni s kratkim razpolovnim časom.
Elementi teh dveh skupin imajo visoko tališče in so vsi trdni pri sobni temperaturi.
Pol kovine
Ti polmetal Vsega skupaj je sedem elementov:
Bor (B)
Silicij (si)
Germanij (Ge)
Arzen (kot)
Antimon (Ponedeljek)
Telur (Te)
Polonij (Po)
Ta razvrstitev je dana elementom, ki imajo fizikalno-kemijske lastnosti, pomembne za kovine, in tudi druge, pomembne za nekovinske elemente. Semimetali imajo sijaj, so krhke spojine, ki lahko tvorijo katione in tudi anione (odvisno od stanja) ter so vmesni prevodniki.
Vrste kovin
Železo: snovi, ki v svoji sestavi vsebujejo železo. So kovinske zlitine ki vsebujejo železo kot skupni element, vendar jih je mogoče formulirati z različnimi koncentracijami ogljik, na primer ali kovani z različnimi tehnikami, tako da imajo izdelke z različnimi fizikalnimi lastnostmi.
Neželezni: zlitine, ki jih tvorijo druge vrste kovin, kot npr aluminij, baker, niklja, cink, titan.
Težke kovine: svinec, nikelj, cink, živo srebro. So reaktivne, strupene in bioakumulativne kovine. Med drugim se uporabljajo v baterijah, svetilkah, strelivu za vojne predmete.
Kemijske vezi kovin
Kovine so elementi elektropozitiven, to pomeni, da imajo težnjo izgubljati elektrone v kemični vezi. Ko kovina sodeluje z nekovino, ta izvedemo ionsko vez zaradi razlike v elektronegativnost. Druga možnost vezave kovin so kovinske vezi.
Ob kovinske povezave se pojavijo med kovinami, z delnim sproščanjem elektronov in tvorbo oblaka ali morja elektronov okoli atomov, kar kovinskim delom zagotavlja lastnosti prevodnost električna in kovnost.
Glej tudi: Vodniki in izolatorji - kakšne so razlike?
Pridobivanje kovin
Večina kovin najdemo naravno v kamnine in minerali, povezani z drugimi elementi. Obstaja več tehnik za prečiščevanje kovin, na primer z elektrolizo in kemičnimi reakcijami na ločene spojine.
Pri kovinah sta v industriji najpogosteje uporabljeni tehniki za doseganje določene stopnje čistosti v kovini: razlika v gostoto in magnetna občutljivost (težnja, da mora kovina reagirati na a magnetno polje).

rešene vaje
Vprašanje 1 - (Enem) Kadmij, ki je prisoten v baterijah, lahko pride do tal, kadar se ti materiali nepravilno odlagajo v okolje ali ko sežgejo. Za razliko od kovinske oblike so ioni Cd2 + izjemno nevarni za telo, saj jih lahko nadomestijo Ioni Ca2 + povzročajo degenerativno bolezen v kosteh, zaradi česar so zelo porozne in povzročajo hude bolečine v kosteh. sklepov. Zavirajo lahko tudi encime, ki jih aktivira kation Zn2 +, ki so izjemno pomembni za delovanje ledvic. Na sliki je prikazano spreminjanje polmera nekaterih kovin in njihovih kationov.
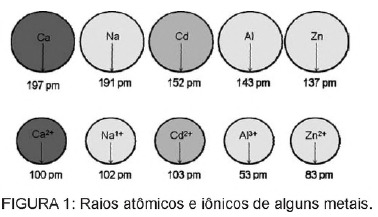
Glede na besedilo je strupenost kadmija v njegovi ionski obliki posledica tega elementa
A) predstavlja nizko ionizacijsko energijo, ki spodbuja tvorbo iona in olajša njegovo vezavo na druge spojine.
B) so nagnjeni k delovanju v bioloških procesih, ki jih posredujejo kovinski kationi z naboji od +1 do +3.
C) imajo polmer in naboj razmeroma blizu kovinskih ionov, ki delujejo na biološke procese in povzročajo interference v teh procesih.
D) imajo velik ionski polmer, ki mu omogoča vmešavanje v biološke procese, v katerih običajno sodelujejo manjši ioni.
E) imajo +2 naboj, ki mu omogoča, da posega v biološke procese, v katerih običajno sodelujejo ioni z nižjimi naboji.
Resolucija
Alternativa C. Kadmij je element, podoben kovinskim ionom, ki jih imamo naravno v telesu. Kadmij se poleg bioakumulacije veže na sulfhidrilne skupine molekul in je podoben kovinskim skupinam. beljakovin, kar povzroča spremembe v bioloških procesih, kot je odstranjevanje vodnega kamna, in uničenje tkiva in rdečih krvnih celic kri.
Vprašanje 2 - Za lastnosti, pomembne za kovine, označite napačno možnost.
A) Večina kovin je dober električni in toplotni vodnik.
B) Nekatere kovine so dovzetne za oksidacijo in / ali redukcijo.
C) Železo je odporna in voljna kovina, to je enostavno oblikovanje.
D) Zemeljskoalkalijske kovine imajo to ime "zemlja", ki se nanaša na okside teh kovin, ki so temne barve.
E) Kovine so elementi različnih barv in dolgočasni zaradi oksidacijskega delovanja.
Resolucija
Alternativa E. Kovine so naravno svetleče in kovinske barve, lahko so oksidacijske, kar povzroči spremembe značilnosti, pomembne za vidik dela, vendar to ni pojav, ki se zgodi pri vseh kovinah, v nekaterih primerih pa je oksidacija odvisna od več dejavnikov zunanji.
avtor Laysa Bernardes
Učitelj kemije