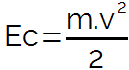je poklican çkisli klorid vsaka organska funkcija, ki izhaja iz reakcije med a karboksilna kislina je organski halid. Spodaj je enačba, ki dokazuje tvorbo kislega klorida in alkohola:

Enačba tvorbe kislega klorida iz karboksilne kisline in organskega halida
Opazimo lahko, da funkcionalna skupina a kisli kloridima karbonil ki so atom klora. V karbonilu imamo tudi organski radikal. Tako lahko funkcionalno skupino kislega klorida povzamemo kot:

Kisli kloridi se pogosto uporabljajo v tako imenovanih organske sinteze, to pomeni, da sodelujejo pri tvorbi drugih organskih spojin, kot so karboksilne kisline, estri in etri. Poleg tega so glavni Lastnosti:
Imajo gostoto večjo od gostote vode;
So polarne spojine zaradi prisotnosti karbonila in atoma klora na koncu verige;
Niso dobro topni v vodi, saj so bolj topni v organskih topilih;
Večina jih je v trdnem stanju pri sobni temperaturi. Vendar pa so kislinski kloridi z nižjo molsko maso praviloma v tekočem stanju.
Imajo nižje tališče in vrelišče kot na primer karboksilne kisline.So izredno reaktivne organske spojine.
Nomenklatura IUPAC za kislinske kloride temelji na naslednjem pravilu:
Klorid + de + predpona + infix + oíla
Primer: Etanoilklorid - Struktura s petimi ogljikovimi atomi (Et), samo enojnimi vezmi (an) in, ker je kisli klorid, se konča z oljem.

Primer: Struktura s petimi atomi ogljika (Pent), samo enojnimi vezmi (an) in, ker je kislinski halid, se konča v olju. Torej imamo pentanoilklorid.

Primer: Struktura s tremi atomi ogljika (Prop), dvojno vezjo (en) in, ker je kisli klorid, se konča v olju. Torej imamo propenoilklorid.

Jaz, Diogo Lopes Dias
Vir: Brazilska šola - https://brasilescola.uol.com.br/quimica/cloretos-acido.htm