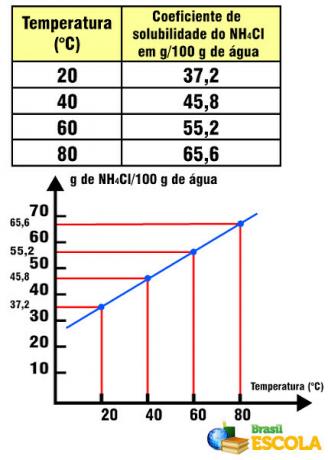
Znanstvenik Friedrich Kohlrausch (1840-1910) je prvi predlagal, da čista voda prevaja elektriko, čeprav v majhnem obsegu. To je zato, ker se voda obnaša amfoterno; to pomeni, da ob določenih priložnostih deluje kot kislina in da protone (H+); v drugih pa se obnaša kot baza in sprejema protone.
To pomeni, da voda izvede svojo ionizacijo v skladu s kemijsko enačbo, prikazano spodaj:
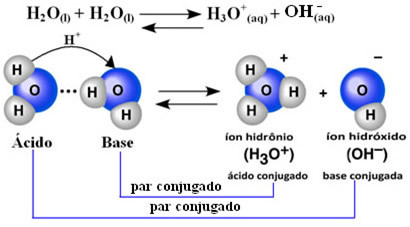
Ta postopek se imenuje avtoionizacija vode in se pojavlja v zelo majhnem obsegu, to je, da je voda zelo šibek elektrolit, z nizkimi vrednostmi stopnje ionizacije in ionizacijske konstante v ravnovesju (Kç). Ravno zato ima voda tako nizko prevodnost.
Da bi dobili idejo, je pri sobni temperaturi 25 ° C mogoče ugotoviti, da so koncentracije hidroksida in hidronijevih ionov, ki nastanejo pri samoionizaciji čiste vode, enake 1. 10-7 mol. L-1. To pomeni, da se od milijarde molekul vode ionizirata le dve.
Imenuje se konstanta ionskega ravnovesja vode çkonstanta disociacije vode,konstanta avtoprotolizeali ionski produkt vode.To konstanto predstavlja Kw, ker se w nanaša na besedo vode, kar v angleščini pomeni voda.
Ne ustavi se zdaj... Po oglaševanju je še več;)
Njen izračun se izvede na enak način kot druge ravnotežne konstante, pri čemer se spomnimo, da, kot je navedeno v besedilu "Konstante Balance Kc in Kp «, v tem primeru bodo v izrazu prikazani samo proizvodi, ker ima voda v tekočem stanju enako aktivnost do 1. Čiste tekoče ali trdne snovi niso vključene v konstanten disociacijski izraz, ker se ne spremenijo. Dajo se samo vodne in plinaste raztopine. Torej imamo:
Kw = [H3O+]. [oh-]
Kw = (1. 10-7). (1. 10-7)
Kw = 10-14
Kot pri drugih ravnotežnih konstantah v reduw spremeni se le s spremembo temperature. S povečanjem temperature vode se povečuje tudi njena ionizacija, kar pomeni, da je samoionizacija vode endotermni proces, torej absorbira toploto.
To je razvidno iz vrednosti ionskega produkta vode (Kw), navedeni v spodnji tabeli pri različnih temperaturah:
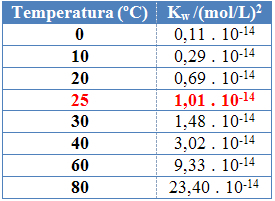
Jonski produkt vode bo imel vedno določeno vrednost pri vsaki temperaturi, bodisi v čisti vodi ali v raztopini. Tudi če ima raztopina koncentracije ionov H3O+ in oh- drugačen bo izdelek med njima ostal konstanten.
Avtorica Jennifer Fogaça
Diplomiral iz kemije
Bi se radi sklicevali na to besedilo v šolskem ali akademskem delu? Poglej:
FOGAÇA, Jennifer Rocha Vargas. "Ionski vodni izdelek (Kw)"; Brazilska šola. Na voljo v: https://brasilescola.uol.com.br/quimica/produto-ionico-Agua-kw.htm. Dostopno 28. junija 2021.