Plin in para
Razlika med plinom in paro je podana iz kritične temperature. Para je snov v plinastem stanju, ki se lahko z naraščajočim pritiskom utekočinja. Plin ni enak. Je tekočina, ki je ni mogoče utekočiniti s preprostim zvišanjem tlaka. Zaradi tega se plin razlikuje od pare.
Obnašanje plinov
Dana snov v plinastem stanju je plin, če je njegova temperatura višja od kritične temperature, če je temperatura enaka ali nižja od kritične temperature, je snov para.
Pravi plini, ki jih običajno poznamo, kot so helij, dušik in kisik, imajo različne in posebne molekularne značilnosti. Če pa jih vse postavimo na visoke temperature in nizke tlake, začnejo kazati zelo podobno vedenje. Pri preučevanju plinov je sprejet preprost teoretični model, ki v praksi ne obstaja, z vedenjem, podobnim vedenju resničnih plinov. Ta približek je boljši, nižji je tlak in višja je temperatura. Ta plinski model se imenuje popoln plin.
Okoli 17. in 19. stoletja so trije znanstveniki (Jacques Charles, Louis J. Gay-Lussac in Paul E. Clayperon) je po preučevanju vedenja plinov izdelal zakone, ki urejajo vedenje popolnih plinov, imenovanih tudi idealni plini. Z njimi določeni zakoni določajo pravila o "zunanjem" obnašanju popolnega plina, ki vodi do šteje le fizikalne veličine, ki so z njimi povezane, to so: prostornina, temperatura in pritisk.
Splošni zakon popolnih plinov
Izraz, ki določa splošni zakon za popolne pline, lahko vidimo takole:
Ne ustavi se zdaj... Po oglaševanju je še več;)
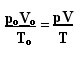
kjer je strO, VO in TO so začetni tlak, začetna prostornina in začetna temperatura. To je izraz, ki se uporablja, kadar se spremenljivke plina razlikujejo.
boyleov zakon
Robert Boyle, fizik in kemik, je bil tisti, ki je določil zakon, ki ureja pretvorbe, ki jih pretvori plin, ko njegova temperatura ostane konstantna. Njegov zakon pravi, da ko je plin podvržen izotermični transformaciji, je njegov tlak obratno sorazmeren zasedenemu volumnu. Iz tega zakona ugotovimo, kako TO = T Moramo:
POVO = pV
Charlesov zakon
Charlesov zakon je zakon, ki ureja pretvorbe popolnega plina v konstantno prostornino. Te transformacije imenujemo izohorne ali izometrične transformacije. Po tem zakonu je pri popolni plinski masi izohorna transformacija njen tlak neposredno sorazmeren z absolutno temperaturo. Matematično lahko ta zakon izrazimo na naslednji način:

kjer je strO in TO so začetni tlak oziroma začetna temperatura.
Gay-Lussacov zakon
Gay-Lussacov zakon je zakon, ki ureja pretvorbe popolnega plina pri stalnem tlaku. Ta zakon je kljub temu, da nosi ime Gay-Lussac, že odkril fizik in kemik A.C.Charles. Po zakonu je količina plina v sorazmerni z absolutno temperaturo izobarna transformacija. Matematično lahko ta zakon izrazimo na naslednji način:

Kjer VO in TO ustrezata začetni prostornini in začetni temperaturi.
Avtor Marco Aurélio da Silva
Poglej več!!
Transformacije plina
Vedeti, kaj so transformacije plinov.
Bi se radi sklicevali na to besedilo v šolskem ali akademskem delu? Poglej:
SANTOS, Marco Aurélio da Silva. "Študija plinov"; Brazilska šola. Na voljo v: https://brasilescola.uol.com.br/fisica/estudo-dos-gases.htm. Dostop 27. junija 2021.