valentna plast je najbolj zunanja plast (ali nivo) (najbolj oddaljena od jedra) atoma, to je tista, ki je najbolj oddaljena od jedra. Zato ima tako imenovane najbolj oddaljene elektrone ali valentne elektrone.
Število ravni, ki jih ima lahko atom, se giblje od 1 do 7, ki imajo naslednje podnivoje (v rumeni barvi):
raven K (1. plast): podnivo s
raven L (2. plast): podnivoji s in P
raven M (3. plast): podnivoji s, P in d
raven N (4. plast): podnivoji s, P, d in f
stopnja O (5. stopnja): podnivoji s, P, d in f
Raven P (6. nivo): podnivoji s, P in d
stopnja Q (1. plast): podnivoji s in P
Vsak od podnivojev ima različno število elektronov. Poglej:
podnivo s vsebuje največ 2 elektrona;
podnivo p vsebuje največ 6 elektronov;
podnivo d vsebuje največ 10 elektronov;
podnivo f vsebuje največ 14 elektronov.
Če je torej valentna lupina določenega atoma M, največje število elektronov, ki jih lahko v njem je 18 (2 elektrona iz s podniveja + 6 elektronov iz p podrazine + 10 elektronov iz podnivo d).
Na dva načina lahko določimo valentno lupino atoma in koliko elektronov ima:
→ Določanje valentne lupine in njenega števila elektronov iz elektronske distribucije
Elektronska distribucija se vedno izvaja prek Diagram Linusa Paulinga, predstavljeni spodaj:

Prikaz diagrama Linusa Paulinga
Vsakdanji atomsko število (kar označuje število elektronov v atomu), opravimo elektronsko distribucijo. Na primer, atom z atomskim številom 50:

Elektronska porazdelitev atoma z atomskim številom, ki je enako 50
Analiziramo zgornjo porazdelitev in ugotovimo, da je raven, ki je najbolj oddaljena od jedra, 5. (N-stopnja), v kateri smo prisotni 4 elektroni (dva v s podravni in 2 v p podnivoju).
→ Določanje valentne lupine in njenega števila elektronov iz periodnega sistema
Tabela je razporejena po obdobjih (vodoravni stolpci), ki označujejo število ravni atoma in skupine ali družine (navpični stolpci). Obdobje se uporablja za določitev valentna plastin družine se uporabljajo za določanje števila elektronov.
a) Poznavanje obdobja kemičnega elementa
Periodni sistem prikazuje skupno sedem obdobij, ki je povezano s številom ravni, ki so prisotne v diagramu Linusa Paulinga. Torej, če poznamo obdobje, v katerem kemični element v tabeli je samodejno, vemo, koliko ravni imajo vaši atomi, valentna plast pa je najbolj oddaljena od jedra.
1. primer: Kemični element Kalij
Kalij je umeščen v četrto obdobje periodnega sistema, zato ima njegov atom štiri ravni, pri čemer je četrta raven valentna plast, kar se potrdi z njeno porazdelitvijo elektronika.
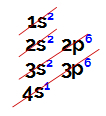
Elektronska distribucija elementa kalija
2. primer: Kemični element Fluor
Fluor je nameščen v drugem obdobju periodnega sistema, zato ima njegov atom dva ravni, druga raven je valentna plast, kar se potrdi z njeno porazdelitvijo elektronika.

Elektronska distribucija fluorovega elementa
3. primer: Indijski kemični element
Indijanec je postavljen v peto obdobje Periodnega sistema, zato ima njegov atom pet ravni, pri čemer je peta raven valentna plast, kar se potrdi z njeno porazdelitvijo elektronika.

Elektronska distribucija elementa indij
b) Poznavanje družine ali skupine kemičnih elementov
Ker poznamo družino ali skupino, v kateri je element, poznamo tudi število elektronov v valentni lupini tega elementa.
Elementi družine A
Elementi družin A so postavljeni v stolpce 1, 2, 13 do 18 Periodne tabele. Vsak od teh stolpcev prejme številko (1 do 8, rimska številka), ki natančno označuje število elektronov v valentni lupini teh elementov:
Stolpec 1 - družina IA = vsi imajo 1 elektron v valentni lupini;
Stolpec 2 - družina IIA = vsi imajo 2 elektrona v valentni lupini;
Stolpec 3 - družina IIIA = vsi imajo 3 elektrone v valentni lupini;
Stolpec 4 - družina IVA = vsi imajo 4 elektrone v valentni lupini;
Stolpec 5 - družina VA = vsi imajo 5 elektronov v valentni lupini;
Stolpec 6 - družina VIA = vsi imajo 6 elektronov v valentni lupini;
Stolpec 7 - družina VIIA = vsi imajo 7 elektronov v valentni lupini;
Stolpec 8 - družina VIIIA = vsi imajo 8 elektronov v valentni lupini.
Oglejte si nekaj primerov določanja števila valentnih elektronov nekaterih elementov družine A:
Primer 1: kemični element barij
Barij se nahaja v družini IIA, zato ima v valentni lupini dva elektrona, kar potrjuje njegova elektronska porazdelitev:

Elektronska distribucija elementa barij
2. primer: Kemični element antimona
Antimon se nahaja v družini VA, zato ima v elektroni valentne lupine pet elektronov, kar potrjuje njegova elektronska porazdelitev:

Elektronska distribucija antimonovega elementa
3. primer: Ksenonski kemijski element
Ksenon se nahaja v družini VIIIA, zato ima v valentni lupini osem elektronov, kar potrjuje njegova elektronska porazdelitev.

Elektronska distribucija ksenonskega elementa
OPOMBA: edini kemični element iz družine A, ki ni v skladu s predlaganim pravilom, je helij. Spada v družino VIIIA, vendar ima v valentni lupini le dva elektrona. To je zato, ker je njegovo atomsko število 2, zato mu je nemogoče imeti 8 elektronov v valentni lupini kot drugi elementi v družini.
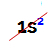
Elektronska distribucija atoma helija
Družinski elementi B
Elementi družin B so postavljeni v stolpcih 3 do 12 Periodnega sistema. Poleg družin A obstaja tudi osem družin B, ki so predstavljene z rimskimi številkami. Za razliko od družin A število družine B ne določa števila elektronov v valentni lupini.
Število elektronov v valentni lupini elementa družine B je vedno enako 2, ne glede na atomsko število in položaj v tabeli. Elektronske distribucije kalifornija (98Prim.) In hassius (108hs) dokažite to:
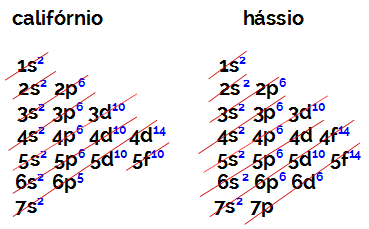
Elektronska distribucija kalifornija ima kot najbolj energetsko podnivo 5f10in o hassius je 6d6. V obeh primerih je podnivo, ki je najbolj oddaljeno od jedra, sedma stopnja in oba imata dva porazdeljena elektrona.
Jaz, Diogo Lopes Dias
Vir: Brazilska šola - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-camada-valencia.htm
