Organske spojine lahko predstavimo na različne načine, kot so ravna strukturna formula, poenostavljena ali zgoščena strukturna formula ali pomišljaj. Vendar je najpreprostejša predstavitev prek molekularne formule.

Poglejmo torej, kako določiti molekulsko formulo organskih spojin na podlagi drugih zgoraj omenjenih formul.
1. Skozi ravno strukturno formulo:ta formula prikazuje razporeditev ali razporeditev atomov znotraj molekule. Na primer, spodaj je ravna strukturna formula enega od ogljikovodikov, prisotnih v bencinu.

Upoštevajte, da so v tej formuli prikazani vsi atomi in vse obstoječe vezi med njimi. Zdaj, če želite določiti molekulsko formulo te spojine, samo preštejte število atomov vsakega elementa in postavite indeks na spodnjo desno stran elementa.
Pomemben vidik, ki ga je treba poudariti, je to molekularno formulo organskih spojin vedno začnemo iz elementa ogljik, saj je glavna sestavina teh snovi. Glej primer:
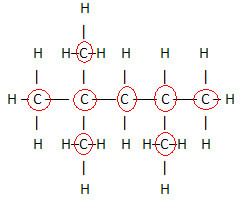
Ker je 8 ogljikov, začnemo molekularno formulo pisati takole: Ç8
Za dokončanje te formule preštejemo količino vodikov:
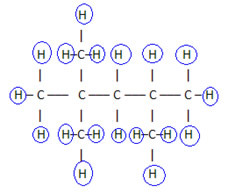
Torej vaš molekulska formula é Ç8H18.
2. Skozi poenostavljeno ali strnjeno strukturno formulo: pri tej vrsti formule je količina vodikov okrajšana. Poglejte na primer isto formulo za molekulo, ki jo najdemo v bencinu, zdaj v zgoščeni obliki:
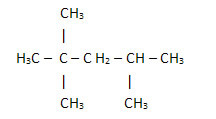
Ne ustavi se zdaj... Po oglaševanju je še več;)
Na ta način je še lažje prešteti količino vodikov, samo dodajte indekse (3 +3+ 3 +2 +1 +3 +3 = 18).
Zdaj pa poglejmo zgoščeno strukturno formulo linolne kisline, ki obstaja v zelenjavi, kot so bombaž, soja, sončnice itd. in ki se uporablja v barvah in lakih:
H3C─CH2CH2CH2CH2CH═CH─CH2CH═CH─CH2CH2CH2CH2CH2CH2CH2─KOOH
Če štejemo količino ogljika, vodika in kisika, imamo naslednje molekulska formula linolne kisline: Ç18H32O2.
3. Skozi formulo kapi: ta formula nadalje poenostavlja predstavitev organskih spojin, saj izpusti skupine C, CH, CH2 in CH3.
Primer je linolna molekula, poglejte, kako izgleda:

Najprej preštejmo količino ogljika in se spomnimo, da je v tej formuli vsaka vez med ogljiki predstavljena s pomišljajem. Tako konice, kot tudi dve točki pregiba, ustrezajo atomom ogljika.
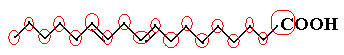
Torej imamo: Ç18
Zdaj, da bi prešteli količino vodikov, se moramo spomniti, da se nakazujejo vezi med ogljiki in vodiki, saj je znano, da ogljik tvori štiri vezi; tako je količina manjkajočih vezi količina vodika, vezana na ta element.
Oglejte si spodnja pojasnila:
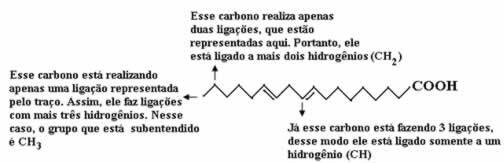
Tako bo količina vodikov: 32.

Količino kisika je povsem enostavno prešteti, saj sta le dva. Ker je molekulska formula é: Ç18H32O2.
Avtorica Jennifer Fogaça
Diplomiral iz kemije
Bi se radi sklicevali na to besedilo v šolskem ali akademskem delu? Poglej:
FOGAÇA, Jennifer Rocha Vargas. "Molekularne formule organskih spojin"; Brazilska šola. Na voljo v: https://brasilescola.uol.com.br/quimica/formulas-moleculares-compostos-organicos.htm. Dostopno 28. junija 2021.
Carbonova prostorska formula, Lewisova elektronska formula, ravninska struktura, elektronski pari, vez kovalentna, valentna plast, razvoj atomskega modela, molekulska formula, strukturna formula, formule tridimenzionalni.
Kemijske formule, ravna strukturna formula, Couperjeva strukturna formula, trojna vez, plin dušik, elektronska formula, Lewisova formula, molekulska formula, enojna vez, dvojna vez, plin ogljikov.



