Pojme reverzibilnih in nepovratnih procesov lahko matematično opišemo s pomočjo koncepta entropije. Toda preden pridemo do definicije entropije, pojdimo na koncepte reverzibilnih in nepovratnih procesov. mi kličemo reverzibilen postopek tisti, pri katerem se sistem lahko spontano vrne v prvotno situacijo (ali stanje). Nepovraten postopek je tisti, katerega sistem se ne more spontano vrniti v prvotno stanje.
Ker so bili koncepti vrst procesov že omenjeni, pojdimo na definicijo entropije. THE entropija sistema (S) je merilo njegove stopnje neorganiziranosti. Večja kot je organizacija, manjša je entropija. Entropija je značilnost termodinamičnega stanja, prav tako notranja energija, prostornina in število molov.
Če pogledamo posode na zgornji sliki, vidimo, da ima posoda 1 a entropija manjši od drugega. Če vzamemo posodo in jo stresemo, bomo preverili, da bodo "kroglice" pomešane ali bolje rečeno neorganizirane. Če preverimo posodo 2, potem ko jo pretresemo, bomo opazili, da za kroglice ni mogoče, spontano se vrnite v prvotno organizacijo, če bomo še naprej stresali posoda.
V reverzibilnih izotermičnih (katerih temperatura vedno ostane enaka) reverzibilnih procesov entropijo definiramo kot razmerje med toploto (dano ali prejeto) in temperaturo. Entropijo torej predstavljamo v izotermičnih procesih na naslednji način:
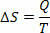
V mednarodnem sistemu enot merimo entropijo v džulih / kelvinah. Na podlagi koncepta, ki ga opisujemo o entropiji, lahko drugi zakon oblikujemo tako:

Sprememba entropije izoliranega sistema je vedno pozitivna ali nična. Enakost ΔS = 0 se pojavi, kadar so procesi reverzibilni: reverzibilni procesi ne povečajo entropije. Izoliranim sistemom, ki niti ne sprejemajo niti ne oddajajo toplote okolju, se lahko entropija le poveča ali ohranja konstantna.
Avtor Domitiano Marques
Diplomiral iz fizike
Brazilska šolska ekipa
Vir: Brazilska šola - https://brasilescola.uol.com.br/fisica/entropia-segunda-lei.htm
