O natrijev klorid (kuhinjska sol) je sol, ki jo v vsakdanjem življenju solimo hrano, pripravljeno na obrt ali predelano (industrializirano). Gre za snov, ki je prisotna tudi v različnih naravnih živilih, ki jih dnevno uživamo, kot so sadje, zelenjava, stročnice, semena itd.
V tem besedilu boste vedeli vse o tej pomembni snovi za vsakdanje življenje človeka:
opredelitev
Natrijev klorid spada v anorgansko funkcijo soli in je sestavljen iz povezave natrijevega kationa (Na+) to je anion ctamoreto (Kl-) prek a ionska vez.
b) Kemijske lastnosti
Natrijev klorid tvorita dva kemična elementa:
→ Natrij (Na):
spada v družino kovin (sposobnih enostavno tvoriti katione) alkalnih (AI);
ima elektron v valentni lupini;
ima atomsko število 11;
ima visoko elektropozitivnost (sposobnost izgube elektronov).
→ klor (Cl)
spada v družino halogenov (VIIA);
je nekovina (zato tako enostavno postane anion);
ima sedem elektronov v valentni lupini;
ima atomsko število 17;
ima visoko elektronegativnost (sposobnost pridobivanja elektronov).
Ker sta prisotna dva kemična elementa, ki tvorita natrijev klorid, sta visoka elektropozitivnost in visoka elektronegativnosti, med njima obstaja ionska vez (vzpostavljena med atomi s težnjo izgube in pridobivanja elektroni).
Kemijsko strukturo natrijevega klorida sestavlja en sam kloridni anion (zelena krogla), ki deluje v interakciji s šestimi natrijevimi kationi (modre krogle), kot je razvidno iz spodnje strukture:
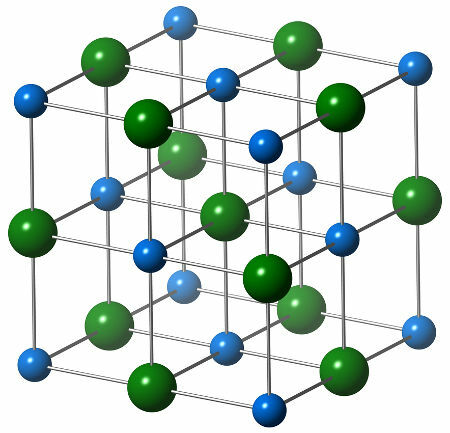
Prikaz kristalne strukture natrijevega klorida
c) Fizične lastnosti
Tališče:
Natrijev klorid se pri temperaturi 801 lahko iz trdnega pretvori v tekoče stanje OÇ.
Vrelišče:
Natrijev klorid se pri temperaturi 1465 lahko pretvori iz tekočega v plinasto stanje OÇ.
Polarnost
Ker gre za snov, ki izvira iz ionske vezi, torej ker je ionska spojina, je natrijev klorid polaren.
Topnost v vodi
Pri 25 l lahko raztopimo v 1 L vode OC, do 359 gramov natrijevega klorida.
Topnost v drugih topilih:
Ker je natrijev klorid polarna spojina, ga ni mogoče raztopiti v nobenem topilu nepolarne narave, kot je olje.
Gostota:
Gostota natrijevega klorida je 2,165 g / ml, zato je gostejša od vode, ki ima gostoto 1 g / ml.
Električna prevodnost:
Ker je ionska spojina, je natrijev klorid sposoben voditi električni tok le, če:
Je v staljenem stanju, to je tekočina;
Raztopljeno v vodi.
d) Načini pridobivanja
Natrijev klorid lahko dobimo fizikalno ali kemično:
1O) Kako postati fizičen:
frakcijska kristalizacija
Natrijev klorid dobimo z izhlapevanjem vode iz oceanov.
podzemni rudniki
V rudnikih se pridobiva z rudarskimi tehnikami.
podzemna nahajališča
Iz globokih podzemnih nahajališč se pridobiva z raztapljanjem v vodi (sol, ki se nahaja v usedlini, se raztopi) in nato črpanjem.
2O) Pridobivanje kemično
sintezna reakcija
Natrijev klorid lahko dobimo s kemično reakcijo sinteze (iz preprostih snovi nastane sestavljena snov) med klorovim plinom in kovinskim natrijem:
2 v(s) + Kl2 (g) → 2 NaCl(s)
Nevtralizacijska reakcija:
Drug način kemičnega pridobivanja natrijevega klorida je reakcija nevtralizacije med klorovodikovo kislino in natrijevim hidroksidom, pri kateri tvorimo sol in vodo:
HCl(1) + NaOH(tukaj) → NaCl(tukaj) + H2O(1)
e) Pomen za ljudi
Natrijev klorid sam po sebi nima funkcije v človeškem telesu, toda ko se disociira na natrijeve katione (Na+) in kloridni anioni (Cl-), ima vsak od teh dveh ionov več pomembnih funkcij za naše telo. Oglejte si nekatere od teh funkcij:
→ Funkcije natrijevega kationa (Na+)
Preprečuje strjevanje krvi;
Se bori proti nastanku ledvičnih in žolčnih kamnov;
Sodeluje pri uravnavanju telesnih tekočin;
Sodeluje pri uravnavanju krvnega tlaka.
→ Funkcije kloridnega aniona (Cl-)
Sodelovanje pri tvorbi in sestavi želodčnega soka (klorovodikova kislina - HCl);
Sodelovanje pri tvorbi soka trebušne slinavke.
f) Poškodbe človeškega telesa
Prekomerno uživanje natrijevega klorida lahko človeku povzroči naslednjo škodo:
→ Škoda, ki jo povzroči presežek natrijevih kationov v telesu:
Povečan čas celjenja ran;
Povečana incidenca krči;
Zvišan krvni tlak;
Preobremenitev ledvic;
Povečano zadrževanje tekočine v telesu.
→ Škoda, ki jo povzroči presežek kloridnih anionov v telesu:
uničenje vitamin E;
Zmanjšanje proizvodnje joda v telesu.
g) druge aplikacije
Poleg tega, da se natrijev klorid uporablja za soljenje hrane, se lahko uporablja tudi v naslednjih primerih:
Proizvodnja šampona;
Proizvodnja papirja;
Proizvodnja Natrijev hidroksid (NaOH);
Proizvodnja detergentov;
Proizvodnja mila;
Sneg se tali v krajih, ki trpijo zaradi neviht;
Proizvodnja kovinskega natrija;
Proizvodnja plina klora;
V izotoniki za nadomestitev elektrolitov v telesu;
V raztopinah za odvajanje nosu;
Proizvodnja fiziološke raztopine; med drugimi aplikacijami.
Jaz, Diogo Lopes Dias

