Obkroženi smo z opremo, ki za delovanje potrebuje celice ali baterije. Vendar pa se veliko teh prenosnih naprav zmanjšuje in s tem prihaja tudi do velike potrebe po miniaturnih baterijah.
Primer te vrste baterij je živosrebrna ali imenovana tudi kup živega srebra in cinka.
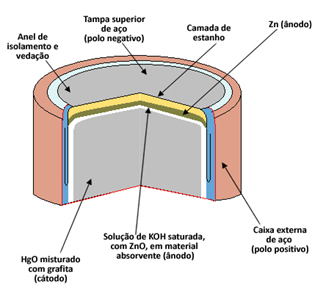
Vsaka celica je sestavljena iz dveh elektrod, anode (negativni pol) in katode (pozitivni pol) ter elektrolita. V primeru živosrebrne celice se anoda tvori kapsula kovinski cink (Zn(s)) to je katoda na živosrebrni oksid II (HgO(s)). Tako Zn kot HgO zmeljemo v prah in stisnemo, da je kup čim manjši. O elektrolit je narejena iz raztopine nasičen kalijev hidroksid (KOH(tukaj)).
Zn oksidira in donira svoje elektrone HgO, kot je prikazano v polreakcijah in globalni reakciji te celice spodaj:
Anodna polovična reakcija: Zn(s) + 2 OH1-(tukaj) → ZnO(s) + 2 H2O(1) + 2e-
Pol reakcija katode: HgO(s) + H2O(1) + 2e- → Hg(1) + 2 OH1-(q)
Globalna reakcija: HgO(s) + Zn(s) → ZnO(s) + Hg(1)
Živosrebrne celice se uporabljajo v digitalnih urah, ročnih urah, fotoaparatih, kalkulatorjih, elektronskih organizatorjih, slušni pripomočki in druge prenosne električne naprave, ki zahtevajo učinkovito delo in trajnost, saj imajo te baterije napetost 1,35V.

Na žalost lahko nepravilno odlaganje teh baterij resno ogrozi okolje, saj vsebujejo živo srebro, ki je težka kovina. Živo srebro lahko onesnaži zemljo, podtalnico, jezersko in rečno vodo ter doseže živali in človeka. Toksičen je tudi v majhnih količinah. Med zdravstvenimi težavami, ki jih lahko povzroči živo srebro, so: poškodbe sluznice, kože, ledvic, močna slabost, bruhanje, bolečine v trebuhu, krvava driska in lahko privede do smrti.
Če želite izvedeti več o tem, zakaj so baterije strupene odpadke, kako je živo srebro kontaminirano in kaj moramo storiti z rabljenimi baterijami, preberite spodaj navedena besedila.
Avtorica Jennifer Fogaça
Diplomiral iz kemije
Vir: Brazilska šola - https://brasilescola.uol.com.br/quimica/pilhas-mercurio.htm
