Ti aldehidi in ketoni so zelo podobne organske funkcije. Oba imata v svoji strukturi karbonilno funkcionalno skupino (C = O), z edino razliko, da v primeru aldehidi, se vedno pojavi na koncu ogljikove verige, to je, da je eden od karbonilnih ogljikovih ligandov vodik; ketoni imajo karbonil med dvema ogljikovima atomoma.
Funkcionalna skupina aldehidi:Funkcionalna skupina ketonov:
O O
║ ║
C C ─ H C C ─ C
Zaradi tega obstajajo primeri funkcionalne izomerije med aldehidi in ketoni. Na primer, spodaj predstavljamo dva funkcionalna izomera z enako molekulsko formulo (C3H6O), vendar je eden aldehid (propanal), drugi pa keton (propanon). Oglejte si, kako to popolnoma spremeni njihove lastnosti in aplikacije:
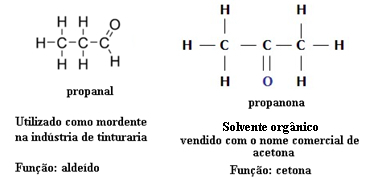
Primer izomerije funkcije med aldehidom in ketonom
Predstavljajte si, da ste v laboratoriju in najdete vialo z brezbarvno tekočino, ki ima le molekulsko formulo C.3H6O. Kako bi ugotovili, ali gre za keton ali aldehid?
Da bi rešili takšne težave, obstajajo metode za razlikovanje aldehidov in ketonov, ki temeljijo na reakciji teh spojin proti šibkim oksidantom
. Kot je prikazano spodaj, ko se soočijo s šibkimi oksidanti, aldehidi reagirajo tako, da oksidirajo, medtem ko ketoni ne reagirajo. Mi to pravimoaldehidi delujejo kot reduktorji, ketoni pa ne, reagirajo le kot reduktorji v stiku z energijskimi oksidanti.Aldehidi + šibki oksidanti → karboksilna kislina
O O
║ ║
C ─ C ─ H + [O] → C ─ C ─ OH
Ketoni + šibki oksidanti → Ne reagirajte
O
║
C ─ C ─ C + [O] → Ne pride do reakcije
Na podlagi tega je dovolj, da izvedemo to reakcijo in preverimo, ali spojina reagira ali ne. Če reagira, vemo, da gre za aldehid; če ne reagira, je keton.
Poleg tega so produkti, ki nastanejo v teh reakcijah oksidacije aldehida, precej vidni, pri čemer pride do sprememb barve, kot bo prikazano kasneje.
Obstajajo tri glavne metode razlikovanja aldehidov in ketonov, in sicer:
1- Tollensov reaktivni: Ta reagent je amonijakova raztopina srebrovega nitrata, tj. vsebuje srebrov nitrat (AgNO3) in presežek amonijevega hidroksida (NH4OH):
AgNO3 + 3 NH4OH → Ag (NH3) OH + NH4PRI3 + 2 H2O
Tollens Reactive (poimenovan po nemškem kemiku Bernhardu Tollensu (1841-1918))
Kot je razloženo v besedilu Izdelava srebrnega ogledala, ko pride aldehid v stik s Tollensovim reaktivnim, se oksidira v ustrezno karboksilno kislino, medtem ko se srebrovi ioni reducirajo na Ag0 (kovinsko srebro). Če to reakcijo izvedemo, na primer v epruveti, se to kovinsko srebro odloži na stene epruvete, kar povzroči nastanek filma, imenovanega srebrno ogledalo. Ta opaženi rezultat je zelo lep in se uporablja v postopku izdelave industrijskih ogledal.
Reakcijo, ki se zgodi, lahko predstavimo na naslednji način:
O O
║ ║
R ─ C ─ H + H2O → R ─ C ─ OH + 2e- + 2 H+
2 Ag+ + 2e- → 2 Ag0
2 NH3 + 2 H+ → 2 NH4+
O O
║║
R C ─ H + 2 Ag+ + 2 NH3 + H2O → R C ─ OH + 2 Ag0 + 2 NH4+
aldehid Tollens reaktivenkarboksilna kislina kovinsko srebro (srebrno ogledalo)
Po drugi strani pa, če keton postavimo v reakcijo s Tollensovim reaktivcem, ne bo prišlo do tvorbe kovinskega srebra, ker ketoni ne morejo zmanjšati Ag-ionov.+.
2- Fehlingov reaktivni: Ta reaktivna reakcija je modra raztopina bakrovega sulfata II (CuSO4) v bazičnem mediju, saj ga zmešamo z drugo raztopino, ki jo tvorita natrijev hidroksid (NaOH) ter natrijev in kalijev tartrat (NaOOC-CHOH-CHOH-COOK). Raztopini bakrovega sulfata II dodamo tartarat, da ga stabiliziramo in preprečimo njegovo obarjanje.
CUSO4 + 2 NaOH → Na2SAMO4 + Cu (OH)2
Fehling Reactive (poimenovan po nemškem kemiku Hermannu von Fehlingu (1812-1885))
V stiku s Fehlingovim reaktivnim faktorjem aldehid tvori karboksilno kislino z njeno oksidacijo, medtem ko bakrovi ioni (Cu)2+), prisotni v sredini, se zmanjšajo in tvorijo rdeče-rjavo oborino (bolj opečnati), ki je bakrov oksid. Ketoni pa ne reagirajo - ker ne morejo zmanjšati ionov Cu2+.
O O
║ ║
R ─ C ─ H + 2 Cu (OH)2 → R ─ C ─ OH + Ass2O + 2 H2O
aldehid rdeče-rjava oborina
3- Benediktova reaktiva: Ta reaktivni del tvori tudi raztopina bakrovega II sulfata (Cu (OH)2) v osnovnem mediju, vendar ga zmešamo z natrijevim citratom.
Tako kot pri Fehlingovem reagentu tudi v primeru reakcije med aldehidom in Benediktovim reagentom obstajajo bakrovi ioni (Cu2+) v mediju, ki so reducirani in tvorijo rdeči bakreni oksid.
Ta reagent se pogosto uporablja v testih za odkrivanje prisotnosti in vsebnosti glukoze v urinu. Glukoza ima v svoji strukturi aldehidno skupino, zato reagira z Benediktovim reagentom, ki je prisoten v trakovih za te teste. Od tam samo primerjajte barvo traku z barvo tehtnice na embalaži izdelka.

Benediktov reagent se uporablja za določanje vsebnosti glukoze v urinu.
Avtorica Jennifer Fogaça
Diplomiral iz kemije
Vir: Brazilska šola - https://brasilescola.uol.com.br/quimica/diferenciacao-aldeidos-cetonas.htm


