Под химическим уравнением понимается описание химических процессов, в котором показаны реагенты и продукты, участвующие в реакции:
C + O2→ CO2
Реагенты продукта
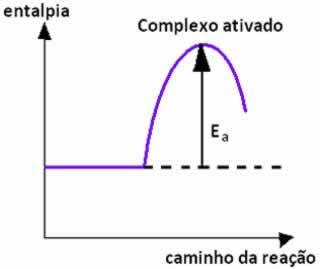
Для возникновения химической связи должен быть разрыв существующих связей в реагентах и образование новых связей в продуктах. Этот процесс включает изучение изменения энергии реакций.
Подача энергии позволяет нарушить связывание реагентов (эндотермический процесс), тогда как образование связей в продукте является экзотермическим процессом, поскольку выделяется энергия.
Энергия связи - это энергия, выделяемая при образовании продукта, и численно равна энергии, поглощаемой при разрыве этой связи, поэтому энергия связи определяется для разрыва связей.
Вкратце: энергия связи - это энергия, поглощаемая при разрыве 1 моля связи в газообразном состоянии при 25 ° C и 1 атм.
См. Теперь пример того, как получить энергию связи реакций:
HCl (г) → H (г) + Cl (г) ∆H = + 103,0 Ккал / моль
Не останавливайся сейчас... После рекламы есть еще кое-что;)
Приведенное выше уравнение показывает, что для разрыва связи на 1 моль молекул HCl (г) и образования 1 моль атомов HCl H (г) и 1 моль атомов Cl (г) необходимы 103,0 Ккал, т.е. энергия связи HCl (г) = + 103,0 Ккал / моль.
Стабильность связи: чем выше энергия связи, тем прочнее связь. Пример:
Если даны следующие энергии связи:
ЧАС2O (1) → H2 (г) + O (г) ∆H = + 110,6 Ккал / моль
HBr (г) → H (г) + Br (г) ∆H = + 88,0 Ккал / моль
Какая связь была бы наиболее стабильной, та, которая присутствует в HBr или в H2О?
Энергия связи воды (H2O) имеет более высокое значение, чем HBr, поэтому он имеет большую стабильность.
Лирия Алвес
Окончила химический факультет
Хотели бы вы использовать этот текст в учебе или учебе? Посмотрите:
SOUZA, Líria Alves de. «Энергия связи в химических уравнениях»; Бразильская школа. Доступно в: https://brasilescola.uol.com.br/quimica/energia-ligacao-equacoes-quimicas.htm. Доступ 28 июня 2021 г.