Реакции галогенирования - это тип реакции органического замещения, то есть реакции, в которых атом или группы атомов заменены атомами или группами атомов другой молекулы органический.
Обычно этот тип реакции происходит с алканами и ароматическими углеводородами (бензолом и его производными).
Галогенирование называется так потому, что оно происходит с простыми веществами галогенов: F2, Cl2, br2 Привет2. Однако наиболее распространенными среди них являются хлорирование (Cl2) и бромирование (Br2), так как фтор очень реакционноспособен, и его реакции взрывоопасны и трудно контролировать, даже разрушая органические вещества:
CH4 (г) + 2 Ж2 (г) → С(s) + 4HF(грамм)
Реакции с йодом очень медленные.
Ниже приведены основные типы галогенирования и некоторые примеры:
1. Галогенирование алканами: Поскольку алканы плохо реагируют, их реакции галогенирования протекают только в присутствии солнечного света (λ), ультрафиолетового света или сильного нагревания. Этот тип реакции проводится для получения галогенида алкила.
Пример: монохлорирование метана:
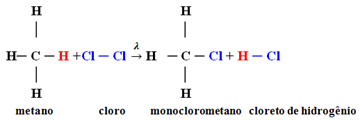
В данном случае это произошло от атома водорода метана (CH4) заменяется атомом хлора, давая монохлорметан. Если бы хлора было слишком много, эта реакция могла бы продолжаться, заменяя все водороды в метане.
1.1. Галогенирование в алканах с более чем 3 атомами углерода: Если реагирующий алкан имеет по крайней мере 3 атома углерода, мы получаем смесь различных замещенных соединений. См. Пример монохлорирования метилбутана ниже:
Не останавливайся сейчас... После рекламы есть еще кое-что;)
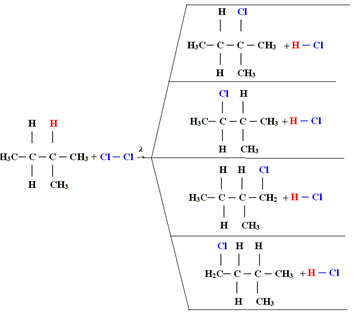
Количество каждого соединения будет пропорционально следующему порядку легкости, с которым водород выделяется в молекулу:

Таким образом, в приведенном выше случае наибольшее количество будет 2-метил-2-хлорбутаном, а наименьшее количество будет 2-метил-1-хлорбутаном.
2. Галогенирование бензола: Бензол обычно не реагирует с хлором или бромом. Однако, если в качестве катализатора используется кислота Льюиса (обычно используется FeCl3, FeBr3 или AlCl3, все в безводной форме) бензол легко вступает в реакцию галогенирования.
Хлорид и бромид трехвалентного железа можно получить, просто добавив в смесь железо, и таким образом оно вступает в реакцию с галогеном и дает кислоту Льюиса:
2 Fe + 3 Br2 → 2 FeBr3
См. Пример галогенирования бензола и его механизм:
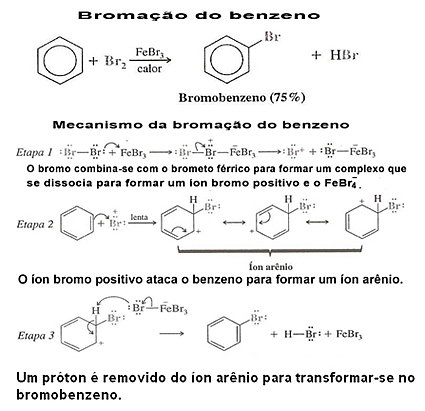
3. Галогенирование производных бензола:В таких случаях замещение определяется заместителем или функциональной группой, которая присоединена к ароматическому ядру. Чтобы увидеть, как это происходит, прочтите тексты "Управляющие радикалы в бензольном кольце" а также "Электронные эффекты мета- и орто-радикалов”.
Дженнифер Фогача
Окончила химический факультет
Хотели бы вы использовать этот текст в учебе или учебе? Посмотрите:
FOGAÇA, Дженнифер Роча Варгас. «Реакции органического галогенирования»; Бразильская школа. Доступно в: https://brasilescola.uol.com.br/quimica/reacoes-organicas-halogenacao.htm. Доступ 28 июня 2021 г.