THE растворимость или коэффициент растворимости, это физическое свойство материи, которое всегда практически определяется в лаборатории. Это связано с емкостью материала, называемого растворенный, представляет быть распущенным другим, растворитель.
Что касается растворимости, растворенные вещества можно классифицировать следующим образом:
Растворимые вещества: те, которые растворяются в растворителе. Например, хлорид натрия (растворенное вещество) растворим в воде (растворителе);
Слабо растворим: те, которые плохо растворяются в растворителе. Это случай гидроксида кальция [Ca (OH)2] (растворенное вещество) в воде;
Нерастворимые: они не растворяются в растворителе. Например, песок (растворенное вещество) не растворяется в воде.
THE растворимость очень связано с приготовлением решения (однородные смеси), поскольку для получения раствора важно, чтобы используемое растворенное вещество было растворимо в растворителе.
Факторы, влияющие на растворимость
Даже если растворенное вещество растворимо в растворителе, существуют некоторые факторы, которые могут влиять на способность растворенного вещества растворяться. Они:
а) Соотношение между количеством растворенного вещества и растворителя
Растворитель всегда имеет предел растворения растворенного вещества. Если мы увеличиваем количество растворителя, сохраняя при этом количество растворенного вещества, растворитель стремится растворить все использованное растворенное вещество.
Б) Температура
Температура - единственный физический фактор, способный изменить растворимость растворителя по отношению к данному растворенному веществу. Эта модификация зависит от природы растворенного вещества, как мы увидим ниже:
эндотермическое растворенное вещество: это тот, который нам удается растворить большую массу, пока температура растворителя выше, чем комнатная температура. Чем горячее растворитель, тем больше растворенного вещества растворяется.
Пример: В горячей воде можно растворить большее количество молотого кофе.
Экзотермическое растворенное вещество: это тот, который нам удается растворить большую массу, пока температура растворителя ниже, чем комнатная температура. Чем холоднее растворитель, тем больше растворенного вещества растворяется.
Пример: Когда сода холодная, возможно растворение большего количества углекислого газа.
Способы определения растворимости
Поскольку растворимость - это свойство, определяемое экспериментальным путем, материалы, как правило, уже оценили свою растворимость в самых разных растворителях. Таким образом, мы можем узнать о растворимости растворенного вещества в определенном растворителе следующим образом:
а) Анализ таблицы
Часто ученик может столкнуться с растворимостью при интерпретации таблицы. См. Следующий пример:
Пример: (UEPG - адаптировано) В таблице ниже показана растворимость соли Li.2CO3 в 100 граммах воды.
Не останавливайся сейчас... После рекламы есть еще кое-что;)

В таблице представлены значения массы в граммах Li2CO3 который можно растворить в 100 граммах воды, от 0 ОС до 50 ОÇ. Мы видим, что чем горячее вода, тем меньше Li2CO3 растворяется. Следовательно, Ли2CO3 это экзотермическое растворенное вещество (оно растворяется больше, если вода холодная).
б) Анализ графика
Растворимость можно оценить, интерпретируя график. Для этого просто определите температуру, поверните ее к кривой, а затем поверните кривую к оси y, которая представляет собой массу растворенного вещества в граммах, которое будет растворено.
Пример: (UFTM - адаптировано) На графике показана кривая растворимости соли AX2.
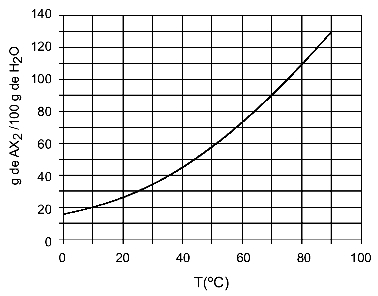
На графике указано, что по оси ординат количество воды (растворителя) составляет 100 граммов. Для растворенного вещества AX2, определим количество воды при следующих температурах:
30ОÇ: Когда включаем температуру 30ОC к кривой, а затем по кривой к оси y, мы имеем, что при этой температуре 100 граммов воды могут растворить примерно 35 граммов растворенного вещества AX.2.
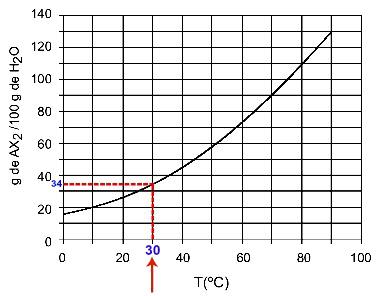
Определение растворимости AX2 в 30ОÇ
40ОÇ: Когда включаем температуру 40ОC к кривой, а затем по кривой к оси y, мы имеем, что при этой температуре 100 граммов воды могут растворить примерно 45 граммов растворенного вещества AX.2.
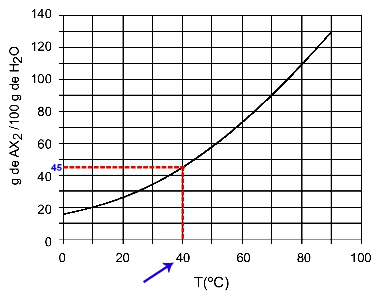
Определение растворимости AX2 в 40ОÇ
Поскольку растворенное количество растворенного вещества увеличивается с каждым повышением температуры, мы получаем, что AX2 это эндотермическое растворенное вещество.
в) текстовая интерпретация
См. Следующий пример:
Пример: (PUC-MG) Некоторые вещества могут образовывать гомогенные смеси с другими веществами. Вещество, которое находится в наибольшем количестве, называется растворителем, а вещество, которое находится в наименьшем количестве, называется растворенным веществом. Хлорид натрия (NaCl) образует гомогенный раствор с водой, в котором можно растворить при 20ºC 36 г NaCl в 100 г воды.
В тексте сказано, что если у нас есть 100 граммов воды (растворителя), при температуре 20 ОC можно растворить до 36 граммов NaCl.
Автор: Диого Лопес Диас
Хотели бы вы использовать этот текст в учебе или учебе? Посмотрите:
ДНИ, Диого Лопес. «Что такое растворимость?»; Бразильская школа. Доступно в: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-solubilidade.htm. Доступ 28 июня 2021 г.
