Аккумулятор это устройство, в котором электрический ток вырабатывается из химической энергии, поступающей от реакция оксидоредукциито есть одна разновидность реагента теряет электроны (окисление), а другая разновидность получает электроны (восстановление).
См. Изображения реакций окисления и восстановления, которые происходят в любом стеке:
Окисление: X → и + X+
Вид X теряет электрон и превращается в катион.
Снижение: Y- + и → Y
анион Y- получает электрон и превращается в нейтральную форму Y.
Основные компоненты стека
Основные компоненты стека:
Анод: отрицательный электрод, в котором происходит реакция окисления, то есть потеря электронов;
Катод: положительный электрод, в котором происходит реакция восстановления, то есть усиление электронов;
Электролитический раствор (солевой мостик) или проводящий материал (например, графитовый стержень): это средство, с помощью которого электроны, отданные анодом, достигают катода.
Основы работы аккумулятора
Функционирование стека происходит от следующих событий:
1-й принцип: Анодное окисление
Металл в аноде, поскольку он имеет большую тенденцию терять электроны, становится катионом, как мы наблюдали в уравнении ниже:
Zn → Zn2+ + 2 и
2-й принцип: катодное восстановление
Катионы, входящие в состав материала, присутствующего в катоде (мы будем использовать в качестве примера медь), при получении электроны с анода превращаются в металлическую медь, как мы можем видеть в уравнении ниже:
Жопа2+ + 2e → Cu
первые сваи
а) Батарея Алессандро Вольта
Задняя часть стопки Алессандро (первая стопка в истории), собранная в 1800 году, была образована вставными металлическими дисками, как на изображении ниже:

Сборка аналогична спине Алессандро к твоей стопке
Диски чередовались, потому что имели разный состав. Один был сделан из металлического цинка, а другой - из меди и всегда отделялся хлопком, пропитанным рассолом (раствором, образованным водой и солью).
Не останавливайся сейчас... После рекламы есть еще кое-что;)
Б) Куча Даниэля
Котел Даниэля, собранный в 1836 году, состоял из двух полуэлементов, соединенных проводящей проволокой и соляным мостиком.
Полуячейка 1: это был анод, то есть отрицательный полюс аккумулятора.
Он состоял из цинковой пластины, и часть этой пластины была погружена в раствор, образованный водой и сульфатом цинка (ZnSO4).
Половина ячейки 2: это был катод, то есть положительный полюс батареи.
Он состоял из медной пластины, и часть этой пластины была погружена в раствор, образованный водой и сульфатом меди (CuSO4).
соляной мост
U-образная трубка, содержащая раствор, образованный водой и хлоридом калия (KCl), соединяла две полуэлементы (цинк и медь) и имела стекловату на обоих концах.
батареи в настоящее время
На данный момент существует несколько моделей стеков, но в целом они выглядят так:
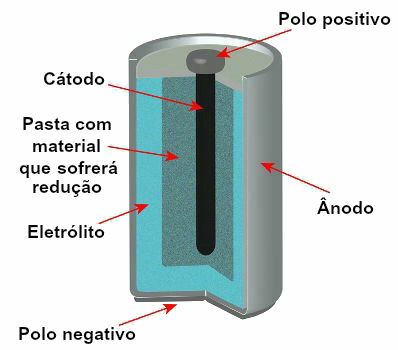
Схема, представляющая модель текущего стека
Наиболее часто используемые модели - это так называемая батарея Leclanché и щелочная батарея, которые имеют следующие отличия:
) Лекланш ворс
Он имеет анод из металлического цинка;
Он имеет катод, образованный пастой с хлоридом аммония, водой, крахмалом и диоксидом марганца;
Он имеет графитовый стержень, который служит проводником для электронов, которые отходят от катода к аноду.
Б) Щелочная батарея
Он имеет анод из металлического цинка или кадмия;
Он имеет катод, образованный оксидом ртути, оксидом никеля и йодом;
Он должен иметь смешанную основу в материале, из которого изготовлен катод.
Автор: Диого Лопес Диас
Хотели бы вы использовать этот текст в учебе или учебе? Посмотрите:
ДНИ, Диого Лопес. «Что такое батарея?»; Бразильская школа. Доступно в: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-pilha.htm. Доступ 27 июня 2021 г.