В энергия активации это минимальное количество энергии, необходимое для того, чтобы столкновение между частицами реагента, сделанными в благоприятной ориентации, произошло и привело к реакции.
Реакции происходят только тогда, когда реагенты имеют энергию активации (или минимальную необходимую энергию, которая варьируется от реакции к реакции; либо по количеству, либо по форме), либо когда он им предоставляется.
Например, когда металлический натрий вступает в контакт с водой, он бурно реагирует. Это означает, что энергосодержание этих реагентов уже достаточно для протекания реакции.
В случае включения печи реакция горения произойдет только в том случае, если мы поместим зажженную спичку или какой-либо другой источник огня рядом с газом, который выделяется из печи. Это означает, что в данном случае необходимо было подать энергию в систему, чтобы она достигла энергии активации, и реакция произошла.
В случае использования самого люминофора для его сгорания энергия активации обеспечивается трением. То же самое происходит с зажигалками, которым также нужна искра, дающая необходимую энергию активации для сгорания содержащегося в них газа.
Энергия активации также может быть получена с помощью света, как в случае разложения перекиси водорода. Поэтому его хранят в темных или непрозрачных бутылках.

Таким образом, можно сделать вывод, что энергия активации (Eдо того как) - это разница между энергией, необходимой для начала реакции (E), и энергией, содержащейся в реагентах (Eпр):

Энергия активации является препятствием для протекания реакции, и она необходима для разрыва связей реагентов. При этом происходит реакция и образуются новые соединения с образованием продуктов.
Когда столкновение между частицами реагентов с благоприятной ориентацией происходит с равным или равным выше, чем энергия активации, до образования продуктов образуется промежуточное и нестабильное состояние, названный комплекс активирован, в котором связи реагентов ослабляются и образуются продуктовые связи. Таким образом, энергия активации - это энергия, необходимая для образования активированного комплекса.
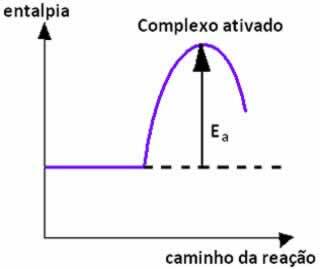
Ниже у нас есть график, который показывает энергию активации как барьер для протекания реакции:
Дженнифер Фогача
Окончила химический факультет
Источник: Бразильская школа - https://brasilescola.uol.com.br/quimica/energia-ativacao.htm


