Изобарическое превращение происходит, когда газ находится под постоянным давлением. Например, если это делается в открытой среде, преобразование будет изобарическим, так как давление будет атмосферным, которое не изменится.
В этом случае меняются температура и объем. Два ведущих ученых изучили, как происходит это изменение изобарических превращений. Первым, кто связал объем и температуру газов, был Жак Шарль (1746-1823) в 1787 году, а затем, в 1802 году, Жозеф Гей-Люссак (1778-1850) количественно оценил это соотношение.
Таким образом, появился закон, объясняющий изобарические превращения газов, который стал известен как закон Шарля / Гей-Люссака. Утверждается следующее:
«В системе с постоянным давлением объем фиксированной массы газа прямо пропорционален температуре».

Это означает, что если мы увеличим температуру вдвое, объем, занимаемый газом, также увеличится вдвое. С другой стороны, если мы уменьшим температуру, объем газа также уменьшится в той же пропорции.
Это можно увидеть в очень простом эксперименте. Если мы поместим воздушный шар в горлышко бутылки, фиксированная масса воздуха окажется в ловушке. Если мы окунем эту бутылку в таз с ледяной водой, воздушный шар сдувается. Теперь, если мы поместим его в таз с горячей водой, воздушный шар наполнится.
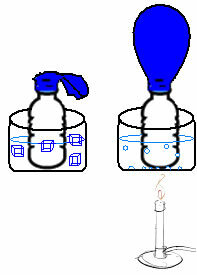
Это связано с тем, что с повышением температуры кинетическая энергия молекул газа увеличивается, а также увеличивается скорость их движения. Таким образом, газ расширяется, увеличивая занимаемый объем, и воздушный шар надувается. Обратное происходит, когда мы понижаем температуру, помещая в холодную воду.
Не останавливайся сейчас... После рекламы есть еще кое-что;)
Это соотношение между температурой и объемом при изобарических превращениях задается следующим соотношением:
V = k
Т
"k" - постоянная величина, как видно на следующем графике:
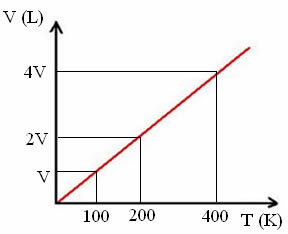
Обратите внимание, что отношение V / T всегда дает постоянную величину:
_V_ =_2V_ = _4V_
100 200 400
Таким образом, для изобарических преобразований можно установить следующее соотношение:
Vисходный = VФинал
Тисходный ТФинал
Это означает, что при любом изменении температуры газа при постоянном давлении мы можем определить его объем с помощью этого математического выражения. Верно и обратное, зная объем газа, мы узнаем, какой он температуры. См. Пример:
«Газообразная масса занимает объем 800 см3 при -23 ° C, при заданном давлении. Какая температура регистрируется, когда газообразная масса при том же давлении занимает объем 1,6 л? »
Разрешение:
Данные:
Vисходный = 800 см3
Тисходный = -23 ºC, прибавив к 273, мы получим 250 K (Кельвин)
VФинал = 1,6 л
ТФинал = ?
* Сначала мы должны оставить громкость на том же устройстве. Известно, что 1 дм3 равняется 1 литру. как 1 дм3 такая же, как 1000 см3, получается, что 1 литр = 1000 см3:
1 л 1000 см3
х 800 см3
х = 0,8 л
* Теперь заменяем значения формулы и находим итоговое значение температуры:
Vисходный = VФинал
Тисходный ТФинал
0,8_ = 1,6
250 тФинал
0,8 тФинал = 250. 1,6
ТФинал = 400
0,8
ТФинал = 500 КБ
* Переходя к шкале Цельсия, мы имеем:
Т (К) = Т (° С) + 273
500 = Т (° C) + 273
Т (° C) = 500 - 273
Т (° С) = 227 ° С
Дженнифер Фогача
Окончила химический факультет
Хотели бы вы использовать этот текст в учебе или учебе? Посмотрите:
FOGAÇA, Дженнифер Роча Варгас. «Изобарическая трансформация»; Бразильская школа. Доступно в: https://brasilescola.uol.com.br/quimica/transformacao-isobarica.htm. Доступ 27 июня 2021 г.
Что такое газы, каковы свойства газов, молекулярные соединения, сжимаемость, фиксированный объем, кинетическая энергия средняя, абсолютная температура газа, идеальный газ, реальные газы, идеальный газ, переменные состояния газа, объем газа, времена года
Химия

Законы Гей-Люссака, Закон Пруста, Химическая реакция, Постоянная пропорция, Масса веществ, Чистое вещество, Анализ качественное и количественное, закон идеальных газов, закон постоянных пропорций, закон определенных пропорций, закон объемный.



