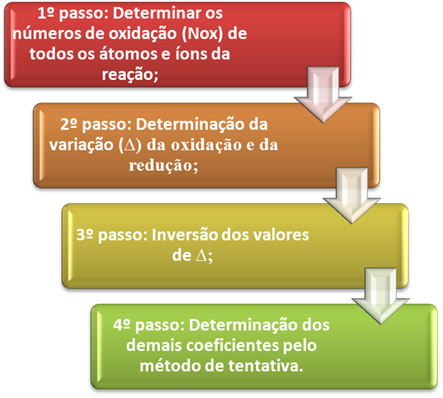
O Расчет Kps (произведение растворимости) связано с двумя химическими равновесиями, которые возникают, когда Трудно растворимый электролит (соль, основание или кислота) образует насыщенный раствор с водой задний план. Два баланса:
равновесие растворения
ИксВYб (здесь) → XВYb (ppt)
В этом балансе скорость растворения электролита в воде равна скорости его осаждения. Константа равновесия (Kc) равна:
Kc = 1
ИксВYб (здесь)
баланс диссоциация
XaYб (здесь) → aX+(здесь) + bY-(здесь)
как электролит растворяется в воде, автоматически он, если диссоциирует, высвобождая катион и анион. В этом случае константа равновесия (Kc) равна:
Kc = [ИКС+]В. [Y-]B
[ИКСВYб (здесь)]
Молярность электролита в растворе всегда постоянна., поэтому мы можем включить его в Kc:
Kc. ШахYb (водн.) = X+ а. Y-B
Включая молярность электролита в Kc, он называется Kps, и молярности (растворимость или коэффициент растворимости) ионов возводятся в их соответствующие показатели степени:
Kps = [X+ а]. [Y-B]
Итак, поскольку Kps связано с ионами, выделяемыми электролитом,
Чтобы разработать расчет этой постоянной, важно знать, что молярность катиона и аниона всегда подчиняется соотношению в молях с молярностью исходного электролита, то есть:CaCl2 → Ca+2 + 2 кл-1
Соблюдая уравнение диссоциации электролита, имеем 1 моль CaCl2 на 1 моль Ca+2 и 2 моля Cl-1. Таким образом, если концентрация CaCl2 для x, что из Ca+2 будет x, а Cl-1 будет 2x.
♦ Примеры расчета Kps
1) (UFRJ) Каким будет выражение Kps CaF2, используя x как молярность соли?
разрешение:
Первоначально необходимо составить уравнение диссоциации соли:
CaCl2 → Ca+2 + 2 кл-1
В уравнении мы имеем 1 моль CaF2 высвобождает 1 моль CaF2 и 2 моля F-1. Следовательно, если молярность соли равна x, молярность Ca+2 будет x и молярность F-1 будет 2x.
С этими данными мы можем составить выражение Kps соли:
Kps = [Ca+2]. [F-1]
Кпс = х. (2x)2
Кпс = х. 4x2
Kps = 4x3
2) (Mackenzie-SP) Определите произведение растворимости (Kps) карбоната кальция (CaCO3), которая имеет растворимость 0,013 г / л при 20OÇ. Данные: Ca = 40; С = 12; О = 16.
разрешение:
Мы должны преобразовать концентрацию, полученную в упражнении, из г / л в моль / л, поскольку это единица измерения концентрации, используемая в расчетах Kps. Для этого рассчитайте молярную массу соли, а затем разделите полученную концентрацию на молярную массу:
Не останавливайся сейчас... После рекламы есть еще кое-что;)
- Расчет молярной массы:
MCACO3 = 40 + 12 + 3.(16)
MCACO3 = 40 + 12 + 48
MCACO3 = 100 г / моль
Преобразование концентрации (C) из г / л в моль / л (М):
M = Ç
MCaCO3
M = 0,013
100
М = 1.3.10-4 Молл
Имея в виду молярность соли, необходимо знать концентрацию каждого из ее ионов на основе их диссоциации:
CaCO3 → Ca+2 + CO3-2
Как моль CaCO3 высвобождает 1 моль Ca+2 и 1 моль CO3-2, концентрация каждого иона будет равна концентрации соли, то есть 1.3.10-4. Наконец, просто вычислите Kps из выражения, составленного из уравнения диссоциации соли:
Kps = [Ca+2]. [CO3-2]
Kps = 1.3.10-4. 1,3.10-4.
Kps = 1,69,10-8 (Молл)2
3) (F.C. Chagas-BA) Растворимость определенного хлорида MCl2 в воде - 1,0. 10-3 Молл. Каким будет значение вашего произведения растворимости:
разрешение:
Это упражнение уже предоставило нам молярность электролита, поэтому достаточно провести его диссоциацию, чтобы определить молярную концентрацию каждого иона и Kps.
MCI2 → M+2 + 2 кл-1
Как 1 моль MCl2 дает 1 моль M+2 и 2 моля Cl-1, молярность M+2 будет равно 1.0.10-3, а тот из Cl-1 будет двойным, то есть 2.0.10-3. Наконец, просто рассчитайте Kps из выражения, составленного из уравнения диссоциации электролита:
Kps = [M+2]. [Cl-1]2
Kps = 1.0.10-3. (2,0.10-3)2.
Kps = 1.0.10-3. 4,0.10-6
Kps = 4,10-9 (Молл)2
4) (OSEC-SP) Произведение растворимости бромида серебра составляет 5,2 × 10-13. Если в растворе содержится 2,0 × 10-2 моль Br-, какой будет максимальная концентрация ионов Ag+(здесь) необходимо, чтобы не осаждать бромид серебра (AgBr)?
разрешение:
Данные, полученные в ходе упражнения:
Kps: 5.2.10-13
[Br-1] = 2.10-2
[Ag+1] = ?
Давайте проанализируем диссоциацию поставляемой соли:
AgBr → Ag+1 + Br-1
Мы знаем, что 1 моль соли дает 1 моль Ag.+1 и 1 моль Br-1. Таким образом, собирая выражение Kps из этих данных, мы можем найти максимальную концентрацию ионов Ag+1:
Kps = [Ag+1]. [Br-1]
5,2.10-13 = [Ag+1].2,0.10-2
[Ag+1] = 5,2.10-13
2,0.10-2
[Ag+1] = 2,6.10-11 Молл
Автор: Диого Лопес Диас
Химия

Диссоциация и ионизация, итальянский ученый Вольта, электрический ток, шведский физик-химик Свант Август Аррениус, теория Аррениус, положительные ионы, катионы, отрицательные ионы, анионы, едкий натр, поваренная соль, полярные молекулы, диссоциация ионный,