Окисление энергии в алкины представляет собой органическую реакцию, которая происходит, когда алкин (углеводород, который имеет тройную связь между двумя атомами углерода) добавляется к кислому раствору с реагент Baeyer (Перманганат калия - KMnO4).
ПРИМЕЧАНИЕ: реакция энергетическое окисление можно проводить с дихроматом калия (K2Cr2О7), а не только перманганат калия.
Всякий раз, когда реакция от происходит энергичное окисление в алкинах, продукты, которые могут возникнуть, являются карбоновые кислоты, вода (единственный элемент, который присутствует в любом из них) и углекислый газ (CO2).
Реагент Байера в кислой среде
Когда реактив Байера смешивается с водой, в присутствии кислота (вещество, способное выделять ионы H+) образование двух оксиды (оксид калия и оксид марганца II) и возникающие атомы кислорода ([O]).

Механизмы энергетического окисления в алкинах
1-й механизм: разрыв тройной связи.
Первоначально тройная связь подвергается атаке возникающих атомов кислорода, образованных реактивом Байера. Эта атака приводит к полному разрыву тройной связи.
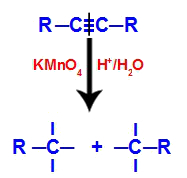
Нарушение тройной связи атакой возникающих атомов кислорода
Когда тройная связь разрывается, алкин разделяется на две части. На каждом из атомов углерода, которые были тройными связями, появляются три свободные валентности.
2-й механизм: Взаимодействие гидроксильных групп
Каждая из свободных валентностей на атомах углерода, где была тройная связь, занята гидроксильными группами (ОН), образуя полиол (алкоголь с несколькими гидроксилами).
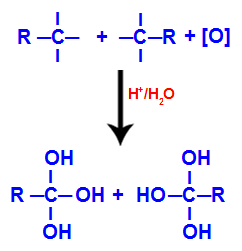
Образование полиола с гидроксильными группами после разрыва тройной связи
ПРИМЕЧАНИЕ: Если к углероду, на котором раньше была тройная связь, присоединен атом водорода, этот атом водорода получит образующийся кислород и также образует другой гидроксил.
3-й механизм: Образование молекул воды
Когда углерод имеет две или более группы ОН, он становится очень нестабильной структурой из-за присутствия чрезвычайно электроотрицательные. Таким образом, из-за нестабильности молекула подвергается самодегидратации, то есть гидроксил связывается с гидроксонием (H+) из другого гидроксила и образует воду.

Образование молекул воды из двух гидроксилов, присутствующих в образованном полиоле.
4-й механизм: Формирование продукта
После образования молекул воды углерод теряет связь из-за выхода гидроксил, и кислород другого гидроксила также теряет связь, которая была сделана с водород. Следовательно, между этим углеродом и кислородом возникает двойная связь, которая образует карбонил (C = O) и стабилизирует оба.
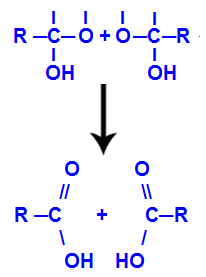
Образование карбонила в двух структурах, полученных из алкина.
Пример уравнения окисления энергии алкинов
Пример: Энергичное окисление Бут-1-ино
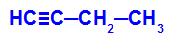
Структурная формула бут-1-ин
Когда бут-1-ин помещается в среду, содержащую реагент Байера, воду и кислоту, связь разрывается. тройка, существующая между атомами углерода 1 и 2, из-за атаки возникающих атомов кислорода, находящихся в середине, как в уравнении ниже:
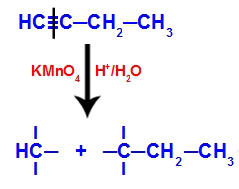
Разрыв соединений бут-1-ин
После разрыва тройной связи атомы углерода 1 и 2 получают три гидроксила, но углерод 1 будет иметь еще один, потому что у него есть атом водорода (который связывается с образующимся кислородом), образуя два полиола (фрагменты 1 и 2).

Уравнение, представляющее образование полиолов
Вскоре после того, как полиолы нестабильны, мы имеем образование молекул воды из гидроксилов. Во фрагменте 1 появляется молекула воды (потому что есть три гидроксила), а во фрагменте 2 появляются две молекулы (потому что гидроксилов четыре).
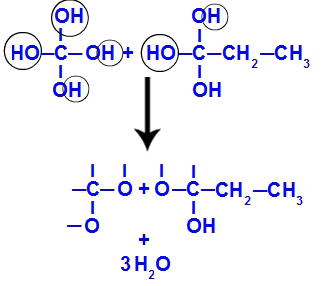
Образование молекул воды из фрагментов бут-1-ин
Наконец, мы имеем образование двойной связи между атомами углерода, потерявшими гидроксил, и атомами кислорода, потерявшими водород, что приводит к образованию карбонилов.

Образование карбонилов в бут-1-иновых фрагментах
С помощью приведенного выше уравнения мы можем видеть, что бут-1-ин дает карбоновую кислоту и диоксид углерода (CO2).
Автор: Диого Лопес Диас
Источник: Бразильская школа - https://brasilescola.uol.com.br/quimica/oxidacao-energetica-alcinos.htm
